题目内容
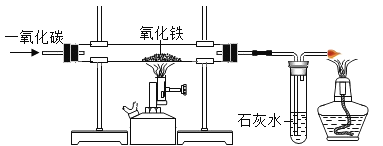
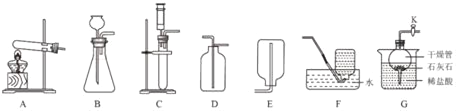
【题目】全国人大和政协会议使用了一种含碳酸钙的“石头纸”。为测定其中碳酸钙(杂质不溶于水,也不与盐酸反应)的含量,某小组的同学进行了如下实验(水和氯化氢的挥发忽略不计):取12.5g样品研碎放入烧杯中,每次加入20.8g稀盐酸后并用电子天平称量,记录实验数据如表:
加入稀盐酸次数 | 1 | 2 | 3 | 4 | 5 |
烧杯及所称物质总质量/g | 82.2 | 101.9 | 121.6 | 141.3 | 162.1 |
(1)“石头纸”中碳酸钙的质量分数为_____
(2)求恰好完全反应时烧杯内溶液中溶质的质量分数____(写出计算过程)
【答案】80% 12.5%
【解析】
(1)由表中实验数据分析可知,第二次放出二氧化碳的质量=20.8g(101.9g82.2g)=1.1g,同理可求得第三次、第四次盐酸都完全反应生成二氧化碳的质量都为1.1g,第五次放出二氧化碳的质量=20.8g(162.1g141.3g)=0g,可知12.5g大理石样品完全反应产生的二氧化碳的质量为1.1g×4=4.4g,假设样品中碳酸钙质量为X,
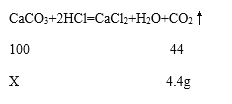
![]() =
=![]() 解得X=10.0g,样品中碳酸钙质量分数=
解得X=10.0g,样品中碳酸钙质量分数=![]() ×100%=80%,写出答:“石头纸”中碳酸钙的质量分数为80%,故填80%;
×100%=80%,写出答:“石头纸”中碳酸钙的质量分数为80%,故填80%;
(2)设反应生成的溶质氯化钙质量为Y,
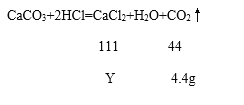
![]() =
=![]() 解得Y=11.1g,溶液质量为纯净的碳酸钙质量和四次加入的稀盐酸质量,还要减去生成的二氧化碳质量,即溶液质量=10.0g+20.8g×4-4.4g=88.8g,氯化钙的质量分数=
解得Y=11.1g,溶液质量为纯净的碳酸钙质量和四次加入的稀盐酸质量,还要减去生成的二氧化碳质量,即溶液质量=10.0g+20.8g×4-4.4g=88.8g,氯化钙的质量分数=![]() ×100%=12.5%,写出答:恰好完全反应时烧杯内溶液中溶质的质量分数为12.5%;故填12.5%。
×100%=12.5%,写出答:恰好完全反应时烧杯内溶液中溶质的质量分数为12.5%;故填12.5%。

练习册系列答案
相关题目