题目内容
【题目】某同学从定量角度研究双氧水制取氧气的过程,对原实验进行部分改进,增加了称量操作.具体做法是:取10%的双氧水和少量的二氧化锰放入气体发生装置,并对反应前后混合物的质量进行称量,记录如下: 若反应后,双氧水分解完全且氧气全部逸出,该同学得出的结论中,不合理的是()
反应过程 | 反应前 | 反应后 |
质量变化(不含容器质量) | 34.3g | 32.7g |
A. 反应速率逐渐加快 B. 最多得到氧气的质量为1.6g
C. 催化剂二氧化锰的质量为0.3gD. 反应得到水和氧气的质量比为9:8
【答案】A
【解析】
A、随着反应的进行,过氧化氢溶液的浓度逐渐减小,故反应速率逐渐变小,故A的结论不合理;
B、根据质量守恒定律,反应前物质的质量总和等于反应后物质的质量总和,生成氧气的质量为:34.3g-32.7g=1.6g,故B结论合理;
C、设生成1.6g氧气需要过氧化氢的质量为x,
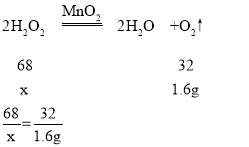
x=3.4g
所以过氧化氢溶液的质量为:3.4g÷10%=34g
二氧化锰的质量为:34.3g-34g=0.3g
故C结论合理;
D、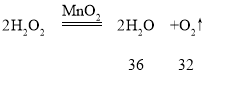
水和氧气的质量比为36:32=9:8,
故D结论合理;
故选:A。

 一诺书业暑假作业快乐假期云南美术出版社系列答案
一诺书业暑假作业快乐假期云南美术出版社系列答案【题目】按要求填写下列内容:
实验过程或方法 | 实验现象 | 结论或解释 |
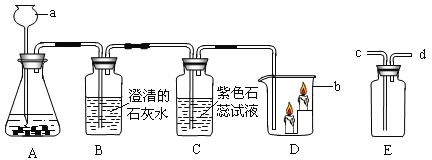
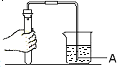
Ⅰ. | 导管口A处有气泡冒出 | ______________________ |
Ⅱ.高锰酸钾制取氧气,用排水法收集。停止加热时,应先: _______, 然后: ________。 | ①为了防止水倒吸入试管,使试管炸裂 ②反应的文字表达式为 _________________; ③试管口略向下倾斜的原因是 _____________________; | |
Ⅲ.将红热的铁丝置于充满氧气并盛有少量水的集气瓶中 | ____________________ | ①反应的文字表达式为 ________________; ②集气瓶盛少量水的作用是 _______________。 |
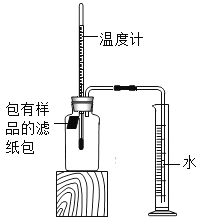
【题目】某化学活动小组探究铁的锈蚀条件过程如下:如图所示(该装置气密性良好),室温时,将包有样品的滤纸包用大头针固定在橡皮塞上,迅速塞紧橡皮塞。已知,此集气瓶净容积为146mL。一段时间后,观察到量筒内水沿导管进入集气瓶。当温度恢复至室温,且量筒内水面高度不再发生变化时读数(此时瓶内氧气含量近似为零)。记录起始和最终量筒的读数以及所需时间如下表。
序号 | 样品 | 量筒起始读数/mL | 量筒最终读数/mL | 所需时间/min |
Ⅰ | 1 g铁粉、0.2 g木炭粉和10滴水 | 100 | 70 | 约120 |
Ⅱ | l g铁粉、0.2 g木炭粉、10滴水和少量氯化钠 | 100 | 70 | 约70 |
根据所学知识推测:
①实验过程中,温度计示数一直升高.
②实验结束后取出Ⅰ号样品滤纸包,打开,可观察到样品的颜色变为红色.
③分析Ⅰ和Ⅱ所得数据,初步推断铁锈蚀的速率与氯化钠有关.
④ 该实验还可测量空气中氧气的含量。根据实验数据计算氧气约占空气体积的21.0%.
⑤ 现要增加一个对比实验,探究木炭对铁锈蚀速率的影响,则需增加实验的样品组成可以为1 g铁粉、0.4g木炭粉和10滴水.
⑥该实验验证了铁生锈是水和氧气等共同作用的结果.
上述正确的判断是:
A. ①②③⑥B. ②③⑥C. ①②④⑤⑥D. ②③