题目内容
【题目】对销售的化肥,国家有明确的质量要求。某兴趣小组对市售的某钾肥进行了检测,称取2.0g样品放入烧杯中,加入适量的水溶解后,逐滴加入10%的BaCl2溶液,产生沉淀的质量与所加入BaCl2溶液质量的关系如图1所示(假定杂质不参加反应)。
已知:K2SO4+BaCl2═BaSO4↓+2KC1。

(1)20.8g BaCl2溶被中所含溶质的质量为_____g。
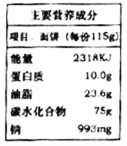
(2)通过计算,判断该钾肥中K2SO4的质量分数是否符合图2的包装说明________?(写出计算过程)
【答案】 2.08 通过计算,该钾肥中K2SO4的质量分数符合图2的包装说明。
【解析】(1)溶质质量=溶液质量×溶质质量分数,则20.8g溶质质量分数为10%的BaCl2溶被中所含溶质的质量为20.8 g×10%=2.08 g。
(2)由图可知生成硫酸钡沉淀的质量为2.33g,设2.0 g样品中硫酸钾的质量为x。
K2SO4+BaCl2═BaSO4↓+2KC1
174 233
x 2.33g
![]() 解得x=1.74g
解得x=1.74g
2.0g样品中硫酸钾的质量分数为![]() ×100%=87.0%,87.0%
×100%=87.0%,87.0%![]() 86.0%,故该钾肥中K2SO4的质量分数符合图2的包装说明。
86.0%,故该钾肥中K2SO4的质量分数符合图2的包装说明。
答:20.8g BaCl2溶被中所含溶质的质量为2.08g,该钾肥中K2SO4的质量分数符合图2的包装说明。

练习册系列答案
相关题目