题目内容
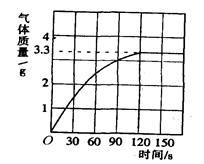
(6分)同学们从山上采集到一种石灰石,他们取100g该样品进行煅烧实验(所含杂质在煅烧过程中不发生变化),其化学方程式为:CaCO3 CaO + CO2 ↑ ,测得反应后固体的质量(m)与反应时间(t)的关系如下表:
CaO + CO2 ↑ ,测得反应后固体的质量(m)与反应时间(t)的关系如下表:
请回答下列问题:
(1)当石灰石完全反应后,生成CO2的质量为 g。
(2)求该石灰石中CaCO3的质量,写出计算过程。
 CaO + CO2 ↑ ,测得反应后固体的质量(m)与反应时间(t)的关系如下表:
CaO + CO2 ↑ ,测得反应后固体的质量(m)与反应时间(t)的关系如下表:| 反应时间t∕s | t0 | t1 | t2 | t3 | t4 | t5 | t6 |
| 反应后固体的质量m∕g | 100 | 92 | 84 | 78 | 72 | 67 | 67 |
(1)当石灰石完全反应后,生成CO2的质量为 g。
(2)求该石灰石中CaCO3的质量,写出计算过程。
(1)33 (2)75g
(1)由实验记录数据可知,在反应进行至t5时,继续煅烧剩余固体质量不再减小,说明碳酸钙已完全分解,根据质量守恒定律,生成二氧化碳的质量=100g-67g=33g
(2)解:设样品中含CaCO3的质量为x
CaCO3 CaO + CO2 ↑
CaO + CO2 ↑
100 44
x 33g
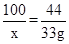
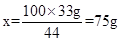
答:石灰石中CaCO3的质量为75g。
(2)解:设样品中含CaCO3的质量为x
CaCO3
 CaO + CO2 ↑
CaO + CO2 ↑ 100 44
x 33g
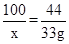
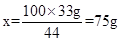
答:石灰石中CaCO3的质量为75g。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目