题目内容
【题目】实验室用10g8%的氢氧化钠溶液和稀硫酸进行中和反应实验,实验过程中溶液的pH变化如图所示:
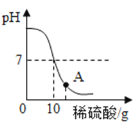
(1)A点溶液的溶质_________。(填化学式)
(2)计算所用的该稀硫酸的质量分数为__________?
【答案】Na2SO4、H2SO4 9.8%
【解析】
(1)因为氢氧化钠与硫酸反应生成硫酸钠和水,所以反应后溶液中溶质有硫酸钠;图中A点pH值小于7,说明硫酸过量,所以溶质中含有过量的硫酸。故答案为Na2SO4、H2SO4。(2)设恰好反应时参加反应的硫酸的质量为x
H2SO4 +2NaOH═Na2SO4 +2H2O
98 80
x 10g×8%
![]()
x=0.98g
该稀硫酸的质量分数为![]() =9.8%
=9.8%
答:该稀硫酸的质量分数为9.8%。

练习册系列答案
 红果子三级测试卷系列答案
红果子三级测试卷系列答案 课堂练加测系列答案
课堂练加测系列答案
相关题目