题目内容
【题目】向盛有10g49%稀硫酸的烧杯中加入5.6g克的铁粉,充分反应后有固体残留,t1时迅速倒入一定量的硫酸铜溶液。整个过程烧杯中溶液的质量随时间的变化如图所示。下列说法正确的是
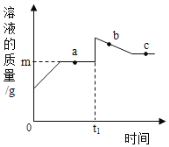
A. 取a点时溶液,加入锌粉,有气体放出
B. b点时,溶液中溶解的物质有两种
C. c点时,烧杯中固体一定是铜
D. 加入铁粉充分反应后的残留固体中有2.8克铁
【答案】BD
【解析】
由方程式:Fe+H2SO4═FeSO4+H2↑
56 98
2.8g 10g×49%
可知,向盛有10g49%稀硫酸的烧杯中加入5.6g克的铁粉,铁粉有剩余,在t1时迅速倒入一定量的硫酸铜溶液,铁与硫酸铜反应溶液的质量减小;A、由上述分析和图象可知,a点时溶液中没有剩余的稀硫酸,加入锌粉,有气体放出,故A错误;
B、由图象可知,b点时溶液的质量还在减小,硫酸铜没有完全反应,溶液中溶质有硫酸亚铁和硫酸铜两种,故B正确;
C、由于硫酸铜的量不能确定,可能有剩余的铁,c点时,烧杯中固体一定是有铜,可能有铁,故C错误;
D、向盛有10g49%稀硫酸的烧杯中加入5.6g克的铁粉,充分反应后残留固体的质量=5.6g-2.8g=2.8g,故D正确。
故选BD。

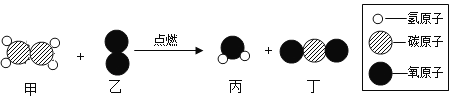
【题目】金属是现代生活和工业生产中应用极为普遍的一类材料。
(一)已知在相同的条件下,金属的活动性越强,金属和酸反应产生气泡(氢气)的速度就越快。Al、Cu、Fe三种金属在稀盐酸里的反应现象如图1所示。

(1)图1中Y所代表的金属是_____(填“Cu”或“Fe”);
(2)Al、Cu、Fe三种金属的活动性由强到弱的顺序为_____;
(3)铝是一种活泼金属,但常温下铝却有较强的抗腐蚀性,其原因是_____;(用方程式表示化学原理)
(二)防止金属腐蚀,特别是钢铁的锈蚀是世界科学研究和技术领域中的重大问题。铁生锈的条件为铁与_____、_____ 同时接触,_____(举一例物质)可加速铁的锈蚀。为了防止铁制品生锈,应采取的措施是_____(写出一种)。
(查阅资料)铁锈成分复杂,化学式可简单表示为Fe2O3nH2O.浓硫酸可以吸水,碱石灰可以吸收水和二氧化碳。
(提出问题)铁锈(Fe2O3nH2O)中n的值等于多少呢?
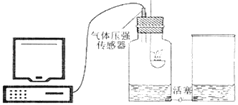
(问题探究)小明发现实验室中有一保管不善的铁粉,大部分已经结块成红褐色,为了探究铁锈(Fe2O3nH2O)的组成,称取27.0g这种铁粉样品,按如图2所示装置进行实验。

(4)实验前应先______。
(5)为了保证实验安全,实验开始时应先_____,目的是_____。
(6)A中的现象是_____,请指出该装置中有一处明显不足_____。
(数据处理)图3是加热时间和A中固体质量关系图象,下表是B、C中质量不再变化时B中浓硫酸、C中碱石灰装置质量变化情况。

反应前(g) | 反应后(g) | |
B | 100 | 105.4 |
C | 150 | 163.2 |
(7)写出T3﹣T4时间段发生反应的化学方程式________。
(8)计算原样品中单质铁的质量分数是______。(计算结果保留1位小数)
(9)n的值是_____。