题目内容
【题目】对乙酰氨基苯酚(C8H9NO2)是速效感冒胶囊的有效成分之一。下列叙述正确的是( )
A. 对乙酰氨基苯酚的相对分子质量是141
B. 对乙酰氨基苯酚中含有2个氧原子
C. 对乙酰氨基苯酚中碳元素的质量分数最大
D. 对乙酰氨基苯酚中,碳、氢、氮、氧元素的质量比是8∶9∶1∶2
【答案】C
【解析】
A. 对乙酰氨基苯酚的相对分子质量是12×8+9+14+2×16=151,选项错误;
B.化学式种元素符号右下角的数字为一个分子中原子的个数,一个对乙酰氨基苯酚中含有2个氧原子,选项错误;
C. 对乙酰氨基苯酚中碳元素的质量分数为![]() ,氢元素的质量分数为
,氢元素的质量分数为![]() ,氮元素的质量分数为
,氮元素的质量分数为![]() ,氧元素的质量分数为
,氧元素的质量分数为![]() ,对乙酰氨基苯酚中碳元素的质量分数最大,选项正确;
,对乙酰氨基苯酚中碳元素的质量分数最大,选项正确;
D. 对乙酰氨基苯酚中,碳、氢、氮、氧元素的质量比是12×8:9:14:2×16=96∶9∶14∶32,选项错误。故选C。

 孟建平小学滚动测试系列答案
孟建平小学滚动测试系列答案【题目】蚊虫叮咬时,会分泌蚁酸.化学小组同学对蚁酸产生了浓厚的兴趣,决定对其进行探究.
[提出问题]蚁酸的成分是什么?它有什么性质?
[查阅资料]I.蚁酸的化学名称叫甲酸,化学式为HCOOH
II.蚁酸隔绝空气并加热时会分解生成两种氧化物
[实验探究](1)向盛有蚁酸溶液的试管中滴加紫色石蕊试液,观察到溶液颜色变成_____色,说明蚁酸显酸性.
(2)小芳同学根据蚁酸中含有_____元素,推测出蚁酸在隔绝空气并加热分解时生成水.
(3)对它分解生成的另一种氧化物,小敏提出两种猜想:
猜想Ⅰ是CO2;
猜想Ⅱ是_____;
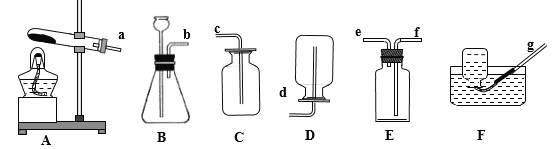
他们按如图所示进行实验:先向装置中通入一会N2,再将蚁酸分解产生的气体通入其中.
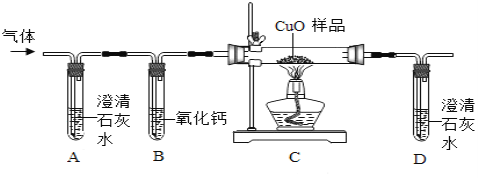
①先通N2的目的是__________;
②若实验过程中看到__________现象,则猜想Ⅰ不成立;
③装置B的作用是__________(用化学方程式表示);
④装置C中的现象为________;
[结论]甲酸受热能分解,反应的化学方程式是_________;
[讨论交流]从环保角度看,该装置存在的明显缺陷是_________.
[拓展延伸]小组同学利用蚁酸分解产生的气体,测定10g氧化铜样品(杂质不参与反应)中氧化铜的质量分数,在不同时刻测定C中固体的质量(如表):
反应时间/min | 2 | 4 | 6 | 8 | 10 |
固体质量/g | 9.3 | 8.8 | 8.5 | 8.4 | 8.4 |
分析表中数据计算:样品中氧化铜的质量分数是多少______?(写出计算过程)