题目内容
【题目】(11分)在宏观、微观和符号之间建立联系是化学学科的特点.
(1)保持氮气化学性质的最小粒子是________,保持汞的化学性质的最小粒子是 ,氯化亚铁溶液中的阳离子是 (均用化学符号表示)。
(2)如下图是钠元素和氯元素在元素周期表中的信息由此信息得出钠原子的相对原子质量为_____;氯原子的核外电子数是______ 。原子序数为17和13的两种元素形成化合物的化学式为 。

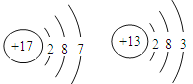
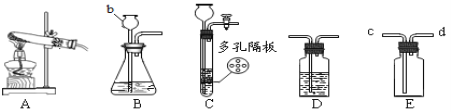
(3)在点燃条件下,甲和乙反应生成丙和丁,反应前后分子变化的微观示意图如下图,甲物质中氮元素的化合价为 ,甲与乙反应的化学方程式为: 。

(4)A、B、C、D表示4种物质,部分物质的微观示意图见下表.A和B在一定条件下反应生成C和D.请回答以下问题:若一定质量的A和4.8g的B恰好完全反应,可生成4.4gC和2.7gD,则A的化学式是______。
物质 | B | C | D |
|
微观示意图 |
|
|
|
【答案】(1)N2 (1分) Hg(1分) Fe2+ (1分)
(2)22.99(1分) 17(1分) AlCl3 (1分)
(3)-3 (1分) 4NH3+3O2 ![]() 2N2 +6H2O (2分)
2N2 +6H2O (2分)
(4)C2H6O (或C2H5OH) (2分)
【解析】
试题分析:(1)氮气有氮气分子构成,N2;汞是金属由汞原子构成,Hg;阳离子带正电,氯化亚铁中带正电的为Fe2+。
(2)单元格中正下方为相对原子质量,因此是22.99;左上角为原子序数,原子序数=质子数=核外电子数,因此是17;原子序数为17,为Cl,最外层电子数为7,易得一个电子,形成Cl-,化合价为-1,原子序数为13,为Al,最外层电子数为3,易失去3个电子,形成Al3+,化合价为+3,那么形成物质的化学式为AlCl3。
(3)甲物质的化学式为NH3,设N的化合价为x,x+(+1×3)=0,x=-3;反应物甲的化学式为NH3,乙的化学式为O2,反应条件点燃,生成物丙的化学式为N2,丁的化学式为H2O;
(4)B4.8g为O2,C4.4g为CO2,D2.7g为H2O,根据质量守恒定律A中含C1.2g、H0.3g、O0.8g,得出C:H:O的个数比=(1.2g÷12):(0.3g÷1):(0.8g÷16)=2:6:1,那么化学式为C2H6O,可以发现就是乙醇C2H5OH。