题目内容
【题目】(6分))下面是某化工厂生产烧碱的工业流程图。
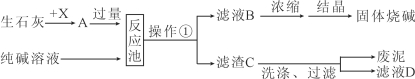
请根据以上信息回答下列问题:
(1)请写出X物质在实验室中的一种用途 。
(2)反应池中发生反应的化学方程式为 。
(3)操作①的名称是 ,结晶得到的固体烧碱中可能含有少量的 (写化学式)。
(4)滤液D可加入反应池循环再利用,目的是降低生产成本和防止 。
【答案】(1)洗涤仪器(或做溶剂或反应物或溶解物质等)
(2)Ca(OH)2+Na2CO3=CaCO3↓+2NaOH (3)过滤 Ca(OH)2 (4) 环境污染
【解析】
试题分析:(1)根据生产烧碱的工业流程图,可判断X物质应是水,在实验室中的一种用途:洗涤仪器(或做溶剂或反应物或溶解物质等)
(2)反应池中发生反应是碳酸钠溶液和氢氧化钙,化学方程式为:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH (3)操作①是将不溶性固体和液体分离,名称是:过滤;由于发生反应:Ca(OH)2+Na2CO3=CaCO3↓+2NaOH,而Ca(OH)2又是过量,故结晶得到的固体烧碱中可能含有少量的:Ca(OH)2
(4)滤液D是洗涤滤渣CaCO3得到的溶液,故滤液D可能含有Ca(OH)2或Na2CO3,可加入反应池循环再利用,目的是降低生产成本和防止环境污染

练习册系列答案
 激活思维优加课堂系列答案
激活思维优加课堂系列答案 活力试卷系列答案
活力试卷系列答案 课课优能力培优100分系列答案
课课优能力培优100分系列答案
相关题目
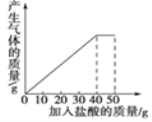
【题目】(6分)石灰石样品的主要成分是CaCO3(已知其它杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到25g该石灰石样品中,得到如下部分数据和图象:
次数 | 第1次 | 第2次 | 第3次 |
加入盐酸的质量/g | 10 | 10 | 10 |
剩余固体的质量/g | 20 | 15 | 10 |
请计算:(1)石灰石样品中杂质的质量为 g。
(2)所加盐酸的溶质质量分数.