题目内容
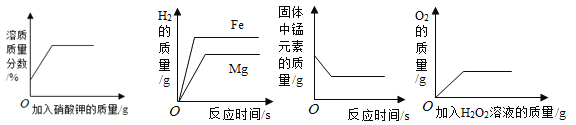
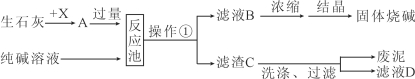
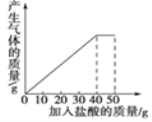
【题目】(6分)石灰石样品的主要成分是CaCO3(已知其它杂质不与盐酸反应).课外小组同学将50g盐酸分5次加入到25g该石灰石样品中,得到如下部分数据和图象:
次数 | 第1次 | 第2次 | 第3次 |
加入盐酸的质量/g | 10 | 10 | 10 |
剩余固体的质量/g | 20 | 15 | 10 |
请计算:(1)石灰石样品中杂质的质量为 g。
(2)所加盐酸的溶质质量分数.
【答案】(1)5 (2)36.5%
【解析】
试题分析:(1)根据图像可知,当加入盐酸的质量为40g时,反应结束,而根据表格中的数据,每加入10g稀盐酸,反应消耗的碳酸钙质量为5g,故当加入盐酸的质量为40g时,恰好反应掉的碳酸钙质量5g×4=20g,故石灰石样品中杂质的质量=25g-20g=5g
(2)根据表格中的数据,前四次都表示所加的稀盐酸与碳酸钙恰好完全反应,故可任取前四次数据来计算,根据化学反应:CaCO3+2HCl==CaCl2+H2O+CO2↑中CaCO3与HCl的质量关系,可求出HCl的质量,进一步计算盐酸的溶质质量分数
解:设HCl的质量为x
CaCO3+2HCl==CaCl2+H2O+CO2↑
100 73
5g x
100:73=5g:x
X=3.65g
盐酸的溶质质量分数=3.65g/10g×100%=36.5%

练习册系列答案
 优学名师名题系列答案
优学名师名题系列答案
相关题目