题目内容
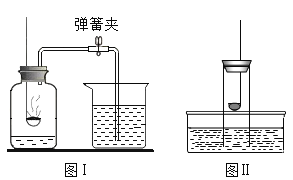
【题目】某化学兴趣小组对教材中“测定空气里氧气含量”的实验(见图I)进行了大胆改进。设计图(II)(选用容积为45mL的试管作反应容器)实验方案进行,收到了良好的效果。请你对比分析下面图I、图II实验,回答下列有关问题:
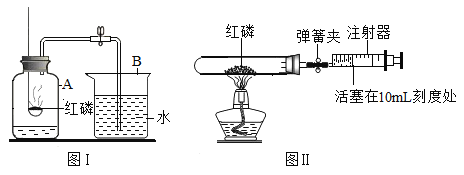
(1)图I实验中红磷燃烧观察到的现象是____。生成物的化学式为____;
(2)图II实验的操作步骤如下:
①点燃酒精灯。
②撤去酒精灯,待试管冷却后松开弹簧夹。
③将稍过量的红磷平装入试管中,将20mL的注射器活塞置于10mL刻度处,并按图II中所示的连接方式固定好,再将弹簧夹紧橡皮管。
④读取注射器活塞的数据。
⑤检查装置气密性
你认为正确的实验操作顺序是____(填序号)。
(3)图II实验中,注射器活塞最终将从10 mL刻度处慢慢前移到约为____mL刻度处才停止。
(4)对照图I实验,你认为图II实验有何优点?(回答一点即可)____。
(5)这个实验除了可以得出氧气约占空气体积的1/5的结论外,还可以推出剩余气体____。(填“易”或“难”)溶于水和其化学性质____(填“活泼”或“稳定”)的结论。
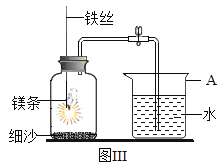
(6)随后该组同学又用镁条来进行实验(如图III所示),实验结束后经测定,结果进入集气瓶中水的体积约为其容积的70%,可能的原因是___。
(7)小明和小芳在讨论“能否用木炭燃烧法来粗略测定空气中氯气的含量”这一问题时,小芳认为:通过图I装置,用木炭燃烧法测得空气中氧气的含量会___(填“偏高”、“偏低”或“无影响”)。她根据木炭燃烧产物的特点阐述了自己的理由:____。
(8)设想用其他物质代替红磷进行实验(图I),则下列因素不会影响实验结果的是(______)
A 替代物能否和氧气反应 B 替代物的用量
C 替代物能否溶于水 D 生成物的状态
【答案】产生大量白烟,放出热量 P2O5 ⑤③①②④ 1 节约药品、误差更小、读数更准确(合理即可) 难 稳定 镁条与空气中其他气体发生了反应 偏低 二氧化碳是气体,不会引起压强的改变 C
【解析】
测定空气中氧气含量实验中,选择的可燃物必须只与氧气反应,且不产生新的气体,才可以引起压强的变化;同时要确保可燃物过量,否则氧气消耗不充分。
(1)红磷在空气中燃烧,产生大量白烟,放出热量,与氧气反应生成的物质是五氧化二磷,化学式为:P2O5。
(2)图Ⅱ实验中,首先需要检查装置的气密性,然后装入药品,再点燃酒精灯将红磷引燃,待反应进行完全后,冷却至室温,最后打开弹簧夹,此时注射器往前移动的距离即为试管内消耗的氧气的量,因此正确的操作顺序应该是⑤③①②④。
(3)空气中氧气的含量约占五分之一,因此容积为45mL的试管作反应容器,瓶内的氧气含量为9mL,故会消耗9mL氧气,从而注射器会从10cm向前移动到1cm处停止前进。
(4)图Ⅰ测量时需要先将红磷在瓶外引燃,而图Ⅱ可以直接在试管内将红磷引燃,误差较小;且注射器带有刻度,可直接准备读数;试管体积更小,可节约红磷用量;故可答误差更小,读数更准确,节约药品等。
(5)红磷燃烧消耗瓶内氧气,不消耗其他气体,因此通过进入集气瓶内的水的体积推测出氧气含量,故剩余气体难溶于水,且化学性质稳定。
(6)进入集气瓶中水的体积约为其容积的70%,超过了氧气的含量1/5,因此可能原因是镁条与空气中其他气体发生了反应。
(7)木炭燃烧产生二氧化碳气体,消耗氧气的同时产生新气体,瓶内气体体积不变化,压强不会减小,因此测定的氧气含量偏低,因为二氧化碳是气体,压强不会改变。
(8)选择的可燃物必须只与氧气反应,且不产生新的气体,才可以引起压强的变化;同时要确保可燃物过量,否则氧气消耗不充分,会产生较大误差,故答案选择C。

 阅读快车系列答案
阅读快车系列答案【题目】氯化钠与硝酸钠的溶解度曲线如图:
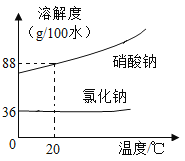
(1)20℃时溶解度较小的物质是______。
(2)从硝酸钠和氯化钠的混合溶液中提纯硝酸钠的方法是_____,可以利用该方法提纯硝酸钠的理由是_____。
Ⅰ.固体混合物中硝酸钠的含量较高,氯化钠的含量较低
Ⅱ.硝酸钠的溶解度受温度影响变化较大
Ⅲ.0℃至100℃,硝酸钠的溶解度始终大于氯化钠
(3)海水中有氯化钠,我们可以利用海水晒盐。某地海水中主要物质的含量见表。
物质 | 每100g海水所含质量(g) |
水 | 96.5 |
氯化钠 | 2.7 |
硫酸钠 | 0.2 |
…… |
①该海水中氯化钠的质量分数为_____。
②20℃时的100g该海水,当水的蒸发量大于____g时,开始析出氯化钠。