题目内容
某化学兴趣小组为了测定黄铜(铜、锌合金)中锌的质量分数,取出6g合金样品,将50g稀硫酸分5次加入样品中,充分反应后过滤、洗涤、干燥、称重,得到的实验数据如下:
(1)m值为 ;
(2)求合金中锌的质量分数?
(3)求稀硫酸中溶质的质量分数?
| 稀硫酸用量 | 剩余固体质量 |
| 第一次加入10g | 4.7 g |
| 第二次加入10g | mg |
| 第三次加入10g | 2.1g |
| 第四次加入10g | 1.2 g |
| 第五次加入10g | 1.2 g |
(2)求合金中锌的质量分数?
(3)求稀硫酸中溶质的质量分数?
(1)m为3.4 (2)80%
(3)设10克稀硫酸中硫酸溶质为X
Zn+ H2SO4===H2↑+ ZnSO4
65 98
1.3g x
65/98=1.3g/x
X=1.96g,
则稀硫酸中溶质的质量分数为1.96g/10g*100%=19.6%
(3)设10克稀硫酸中硫酸溶质为X
Zn+ H2SO4===H2↑+ ZnSO4
65 98
1.3g x
65/98=1.3g/x
X=1.96g,
则稀硫酸中溶质的质量分数为1.96g/10g*100%=19.6%
通过表格可以看出第一次固体溶解了6-4.7=1.3g,所以第二次也应该溶解1.3克,所以m的值为4.7-1.3=2.4,第四次加入10克酸后,它只溶解了2.1-1.2=0.9克,而且第5次剩余固体还是1.2克,说明这1.2克是铜(铜不与酸反应),则6克合金中锌的质量为6-1.2=4.8,则合金中锌的质量分数为4.8g/6*100%=80%.通过表格可以看出10克酸可以溶解1.3克锌,所以根据1.3克锌就可以求出10克稀硫酸中硫酸溶质了。

练习册系列答案
相关题目
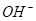 的数量有关;一定体积的溶液中
的数量有关;一定体积的溶液中