题目内容
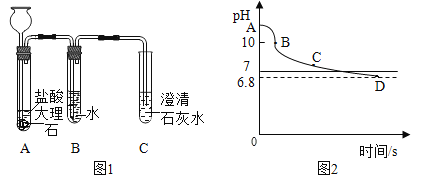
【题目】小红利用氧气、二氧化碳传感器在装有两支燃着的高低蜡烛的密闭容器内顶部测容器内两支蜡烛从点燃到全部熄灭后,氧气(上)和二氧化碳(下)的浓度变化,如图所示。最终剩余氧气浓度15.65%,CO2浓度1.89%.则下列说法不正确的是( )

A. 支持蜡烛燃烧的氧气浓度须达到21%
B. 点B时两支蜡烛全部熄灭
C. 曲线BC段因为蜡烛熄灭,温度下降,二氧化碳密度大下沉,氧气上浮
D. 容器内高的蜡烛先熄灭矮的蜡烛后熄灭
【答案】A
【解析】
空气中氧气的浓度为21%.蜡烛燃烧放出了大量的热,气体受热密度减小,根据容器内空气中氧气和二氧化碳的浓度的变化分析蜡烛燃烧的情况。
A、由密闭装置内气体的变化可知,支持蜡烛燃烧的氧气浓度不一定达到21%,故A错误;
B、点B时氧气的浓度不再减小,说明了两支蜡烛全部熄灭,故B正确;
C、曲线BC段因为蜡烛熄灭,温度下降,二氧化碳密度大下沉,氧气上浮,故C正确;
D、由于气体受热时气体膨胀、密度减小,所以容器内高的蜡烛先熄灭矮的蜡烛后熄灭,故D正确。
故选:A。

 阅读快车系列答案
阅读快车系列答案【题目】小明在实验室里围绕着“盐的性质”这一主题进行了如下的实验探究
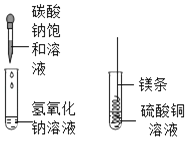
甲 乙
(1)甲实验中反应的化学方程式为_______;
(2)乙实验观察到的现象是_______。
(3)实验后,小明把甲、乙反应后的溶液倒入同一烧杯,发现有白色沉淀生成,他决定对白色沉淀的成分进行探究(提示:本题中碳酸镁视为沉淀处理)
(提出猜想)白色沉淀为:猜想Ⅰ_______;
猜想Ⅱ:Mg(OH)2和BaSO4;猜想Ⅲ:Mg(OH)2和MgCO3;
猜想Ⅳ:Mg(OH)2、MgCO3和BaSO4
小红认为猜想Ⅳ一定不成立,其理由是_______。
(实验方案)
实验操作 | 实验现象与结论 |
过滤、洗涤白色沉淀备用;向白色沉淀中加入盐酸至过量 | ①若_______,猜想Ⅰ成立;其化学反应方程式为_______。 ②若_______,猜想Ⅱ成立。 ③若_______,猜想Ⅲ成立。 |
(拓展与思考)
如果猜想Ⅲ成立,产生此结果的原因是做甲实验时_______。
【题目】已知X和Y作用可生成Z:2X+Y=2Z。使不同质量的X、Y作用,生成Z,各物质质量记录如下表。若每次实验均至少有一种反应物用尽,则下列说法正确的是( )
实验编号 | X(g) | Y(g) | Z化合物(g) |
甲 | 1 | 10 | 5 |
乙 | 2 | 10 | 10 |
丙 | 3 | 10 | 12.5 |
丁 | 4 | 16 | m |
戊 | 5 | 16 | n |
A. 实验乙中,若再添加X,产生Z的质量也不会增加
B. 实验丙中,X和Y均恰好用尽
C. 实验丁中,若再添加Y,产生Z的质量会增加
D. 实验戊中,n的数值为20