题目内容
【题目】为测定一瓶由Na2CO3 、NaOH组成的固体混合物中NaOH的质量分数,小明采用沉淀法进行如下操作:①取20克样品于烧杯中,加足量水配成溶液;②在样品溶液中加入过量的BaCl2溶液;③待反应完全后,过滤、洗涤、干燥、称量。有关数据记录如下表:
反应前 | 反应后 | |
烧杯和样品 溶液总质量/g | 加入的氯化钡 溶液质量/g | 过滤后烧杯和溶液总质量/g (滤液的损失忽略不计) |
95 | 65 | 140.3 |
请回答下列问题:
(1)反应共生成沉淀_____g,原样品中NaOH的质量分数是多少________?
(2)在反应前后的溶液中,下列元素质量保持不变的是_____。
A 钠元素 B 碳元素 C 钡元素 D 氧元素
(3)实验操作步骤③中,确定沉淀洗涤干净的方法:取最后一次洗涤液,滴加_____试剂,观察到_____现象,则已洗涤干净。
【答案】19.7g 47% A 酚酞 不变红
【解析】
(1)反应生成碳酸钡沉淀的质量为:95g+65g-140.3=19.7g,
设样品中碳酸钠质量为x
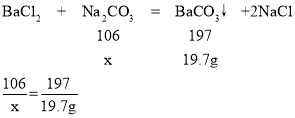
x=10.6g,
原样品中 NaOH 的质量分数是:![]()
答:原样品中 NaOH 的质量分数是47%。
(2)由于反应前后钠元素都是以离子形式存在,没有减少,所以在反应前后的溶液中,元素质量保持不变的是钠元素;故选:A。
(3)氢氧化钠溶液能使酚酞溶液变红,实验操作步骤③中,确定沉淀洗涤干净的方法:取最后一次洗涤液,滴加酚酞试剂,观察到溶液不变红现象,则已洗涤干净。故填:酚酞;不变红。

练习册系列答案
 阅读快车系列答案
阅读快车系列答案
相关题目
【题目】下列除去杂质(少量)的方法中正确的是( )
选项 | 物质 | 杂质 | 除杂方法 |
A |
| CaO | 加足量稀盐酸,过滤 |
B |
|
| 加铜片,过滤 |
C |
| 稀盐酸 | 加过量碳酸钙,过滤 |
D | NaCl固体 |
| 配成热饱和溶液,降温结晶、过滤、洗涤、干燥 |
A.AB.BC.CD.D