题目内容
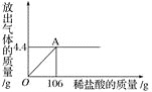
【题目】欲测定盐酸与氯化钙的混合溶液中氯化钙的质量分数,进行了如下实验:取混合溶液100g于锥形瓶中,向其中逐渐加入一定溶质质量分数的碳酸钠溶液(如图一),并不断测定锥形瓶中溶液的pH.反应过程中所得溶液的pH与锥形瓶中物质的总质量的关系如图二所示。
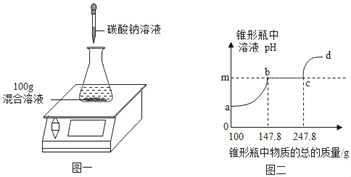
其中,当锥形瓶中溶液的质量增加至147.8g时,共消耗碳酸钠溶液的质量为50g。(忽略二氧化碳在水中溶解的量;氯化钙溶液显中性。)
(1)m点的数值是___。
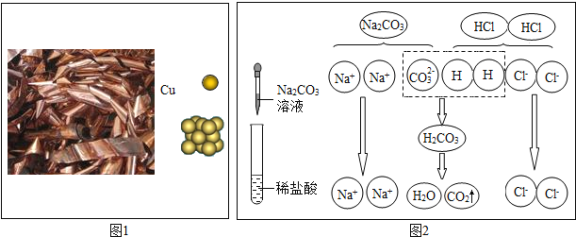
(2)a﹣b段表示碳酸钠与混合溶液中的___反应。
(3)b点的溶质为___。
(4)参加反应的碳酸钠溶液的溶质的质量分数是___。(写出计算过程)
(5)请计算原混合溶液中CaCl2的质量分数为___。(写出计算过程)
【答案】7 HCl 氯化钠和氯化钙 10.6% 11.1%
【解析】
反应开始是盐酸和碳酸钠反应,所以pH值慢慢增大,当盐酸反应完毕,此时pH=7,然后氯化钙和碳酸钠反应,pH保持不变,氯化钙反应完毕后由于碳酸钠溶液显碱性,所以pH继续变大,所以m=7。a﹣b段表示碳酸钠与混合溶液中的 HCl反应。b点是盐酸和碳酸钠恰好完全反应,此时的溶质为生成的氯化钠和尚未参加反应的氯化钙。设参加反应的碳酸钠溶液的溶质质量分数为x,当锥形瓶中溶液的质量增加至147.8g时,共消耗碳酸钠溶液的质量为50g,即消耗的碳酸钠的质量为50g,而溶液质量变化量即生成二氧化碳的质量:100g+50g﹣147.8g=2.2g
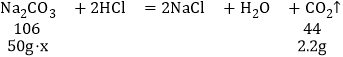
![]()
![]() 解得x=10.6%
解得x=10.6%
由于与氯化钙反应的碳酸钠溶液的质量为247.8g﹣147.8g=100g,则消耗的碳酸钠的质量为100g×10.6%=10.6g
设原混合溶液中CaCl2的质量分数为y
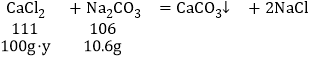
![]() ,解得y=11.1%
,解得y=11.1%
答:(1)m点的数值是7。
(2)a﹣b段表示碳酸钠与混合溶液中的盐酸反应。
(3)b点的溶质为氯化钠、氯化钙。
(4)参加反应的碳酸钠溶液的溶质的质量分数是10.6%。
(5)请计算原混合溶液中CaCl2的质量分数为11.1%。