题目内容
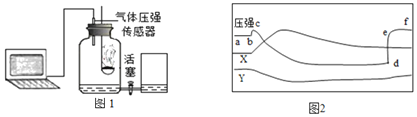
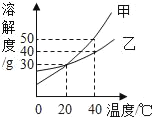
【题目】甲、乙两种固体物质的溶解度曲线如图所示。下列说法正确的是( )
A. 20℃时,甲溶液一定比乙溶液浓
B. 将40℃时甲的一定量饱和溶液降温至20℃,溶液质量不变
C. 甲的溶解度大于乙的溶解度
D. 40℃时,分别在100 g水中各加入30 g甲、乙,同时降温至20℃,甲、乙溶液均为饱和溶液
【答案】D
【解析】
20℃时,是交点,表示甲、乙溶解度相等,饱和时溶质的质量分数一样大,将40℃时甲的一定量饱和溶液降温至20℃,有晶体析出, 溶液质量减少,
A、20℃时,甲溶液一定比乙溶液浓错误,饱和时溶质的质量分数一样大,故A不正确;
B、将40℃时甲的一定量饱和溶液降温至20℃,有晶体析出,溶液质量减少,故B不正确;
C、甲的溶解度大于乙的溶解度错误,因为没有指明温度,故C不正确;
D、40℃时,分别在100g水中各加入30g甲、乙,同时降温至20℃,此温度下甲乙溶解度相等,都为30g,则此时甲、乙溶液均为饱和溶液,故D正确。故选D。

 名校课堂系列答案
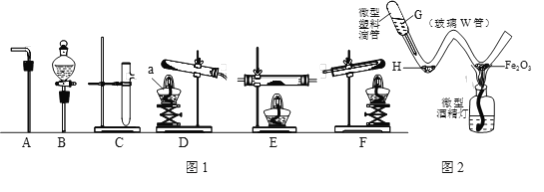
名校课堂系列答案【题目】实验是进行科学探究的重要方法,下列实验设计能实现其对应实验目的是( )
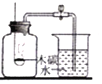
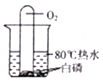
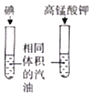
A.验证质量守恒定律 | B.测定空气中氧气含量 | C.验证燃烧需要温度,达到着火点 | D.探究影响某些物质溶解性的因素 |
|
|
|
|
A. AB. BC. CD. D
【题目】在探究金属与酸的反应时,发现铜片与20%的硫酸溶液不反应。有同学提出疑问“在一定条件下铜与硫酸能否发生反应”,并进行了系列实验。
(查阅资料)SO2能让红色的品红溶液褪色,能被NaOH溶液吸收。
(进行实验)(夹持仪器略)
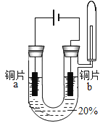
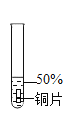
实验1:初步实验(所用溶液均为硫酸溶液)
实验序号 | 1﹣1 | 1﹣2 | 1﹣3 | 1﹣4 | 1﹣5 |
装置 |
|
|
|
|
|
主要现象 | 铜片a附近溶液逐渐变蓝,铜片b附近产生无色气泡。 | 无明显现象 | 无明显现象 | 无明显现象 | 铜片溶解,溶液变蓝,生成有刺激性气味的无色气体 |
经检验实验1﹣1中产生的气体是氢气。
实验2:在实验1﹣5的基础上深入探究,装置如图。

(解释与结论)
(1)实验1﹣1中,能证明铜发生反应的现象是_____。
(2)实验1中,欲得出“升高温度可使铜与硫酸反应”需对比的实验是_____(填实验序号)。
(3)补全实验1﹣5和实验2中铜与硫酸反应的化学方程式:![]() _____
_____
(4)与实验1﹣5相比,实验2的优点有_____(写出一条即可)。
(5)通过上述实验能得出的结论是_____。
(反思与评价)
(6)下列说法不正确的是_____。
A 对比实验1﹣2和1﹣5,可得出“增大浓度可使铜与硫酸反应”
B 通电可促进一些化学反应的发生
C 铜与硫酸只能发生一种化学反应