题目内容
【题目】下图是甲、乙、丙三种固体物质的溶解度曲线,回答下列问题:
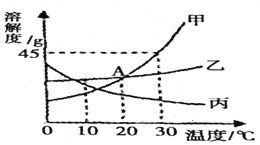
(1)A点的含义是______。
(2)在30℃时,向30克甲物质中加人50克水.充分溶解后所得溶液是______溶液 (填" 饱 和”或“不饱 和” )。
(3)若乙中混有少量甲,最好采用______的方法提纯乙(填“降温 结晶”或“蒸 发 结 晶” )。
(4)将30℃时甲、乙、丙三种物质的饱和溶液降温到10℃,则其溶质质量分数不变的物质是______。
【答案】 20℃时甲乙两种物质溶解度相同 饱和 降温结晶 丙
【解析】(1)据图可以看出,A点表示在20℃时,曱乙两种物质的溶解度相等;(2)在30℃时,甲的溶解度为45g,向30克甲物质中加入50克水,只能溶解22.5g,故充分溶解后所得溶液是饱和溶液;(3)乙的溶解度随温度的升高变化不大,故乙中混有少量甲,最好采用蒸发结晶的方法提纯乙;(4)将30℃时甲、乙、丙三种物质的饱和溶液降温到10℃,乙的溶解度比甲大,则乙溶液溶质质量分数比甲大,丙的溶解度随温度的降低而减小,故溶液组成不变,故其溶质质量分数不变的物质是丙,且小于甲。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】铜镁合金具有优良的导电性,常用作飞机天线等导电材料。科研小组欲测定合金的组成(其他元素忽略不计),进行如下实验:取铜镁合金10 克放入烧杯,将140克稀硫酸分4次加入烧杯中,充分反应后,测得剩余固体的质量,数据记录如表,请计算:
次数 | 1 | 2 | 3 | 4 |
加入稀硫酸质量/克 | 35 | 35 | 35 | 35 |
剩余固体质量/克 | 8.8 | 7.6 | 6.4 | 6.0 |
(1)合金中镁与铜的质量比为_____。
(2)所加稀硫酸的溶质的质量分数______________。(写出计算过程)
【题目】水是生命的源泉,也是不可缺少的资源。
(1)某矿泉水的主要矿物质成分及含量如表:
成分 | Ca | K | Zn | F |
含量(mg/L) | 20 | 3 | 0.06 | 0.02 |
这里Ca、K、Zn、F是指_____ (填“单质、元素、分子或原子”)。
(2)水污染日益严重,水资源的保护和合理利用已受到人们的普遍关注。请参与讨论下列有关问题:
(Ⅰ)检验某地下水是硬水还是软水,可用的物质是_____;实验室常用_____的方法来降低水的硬度
(Ⅱ)某学校饮水处可以将自来水净化为饮用水,其中处理步骤如图所示:
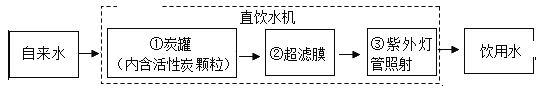
①对应的作用是_____(填字母序号)③对应的作用是_____。
A.杀菌消毒 B.吸附杂质 C.沉淀过滤 D.蒸馏
(Ⅲ)下列做法会造成水体污染的有_____。
A.工业废水直接排放 B.工业废气处理后排放
C.禁止使用含磷洗衣粉 D.大量使用化肥、农药