题目内容
【题目】
A. A B. B C. C D. D
【答案】B
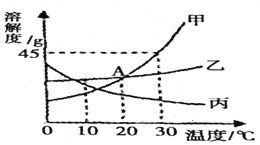
【解析】A、向一定量的氢氧化钠溶液中滴加稀盐酸,该过程中碱不断消耗而使溶液碱性不断减弱,恰好反应时pH=7,直至过量pH小于7,生成水,导致pH最终大于2,故错误;B、生石灰和水反应生成氢氧化钙并放出大量的热,因为氢氧化钙的溶解度会随温度的升高而降低,所以生石灰和水反应过程中氢氧化钙的溶解度减小,氢氧化钙析出,水又减少,导致溶液的质量分数减小,待反应完成后,热量逐渐散失,恢复到原来温度,还是饱和溶液,其溶质质量分数又恢复到原来的数值,故正确;C、向盐酸的氯化铜溶液中滴加氢氧化钠溶液,盐酸先和氢氧化钠反应,故一开始不会出现沉淀,故错误;D、等质量的活泼金属与足量的酸反应生成氢气的多少与![]() 有关,此比值越大,产生的氢气越多,Zn:
有关,此比值越大,产生的氢气越多,Zn:![]() =
=![]() ;Mg:
;Mg:![]() =
=![]() ,可见镁生成的氢气多,又因为镁比锌活泼,反应速度快,故正确。故选B。
,可见镁生成的氢气多,又因为镁比锌活泼,反应速度快,故正确。故选B。

 期末冲刺100分创新金卷完全试卷系列答案
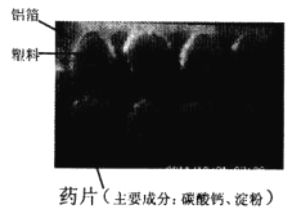
期末冲刺100分创新金卷完全试卷系列答案【题目】小明发现生物老师将一勺白色粉末加入鱼缸后,水中有气泡产生,奄奄一息的鱼很快就活蹦乱跳,于是对这种“白色粉末”产生兴趣,与小刚一起进行了相关探究。
(1)实验准备
①查阅资料:白色粉末的主要成分是过碳酸钠(Na2CO4),常温下与水反应生成氧气。
②用一定溶质质量分数的NaOH和Na2CO3两种溶液进行如下实验。
NaOH溶液 | Na2CO3溶液 | |
滴加酚酞溶液 | 溶液变红色 | 溶液变红色 |
加入稀盐酸 | 无明显现象 | 现象Ⅰ |
加入澄清石灰水 | 无明显现象 | 现象Ⅱ |
加入 1%的CaCl2溶液 | 溶液变浑浊 | 溶液变浑浊 |
加入 0.1%的CaCl2溶液 | 无明显现象 | 溶液变浑浊 |
表中的现象Ⅰ为_____________,现象Ⅱ对应的化学反应方程式为_____________。
(2)实验过程
实验1:检验气体
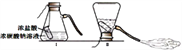
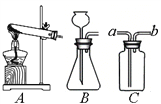
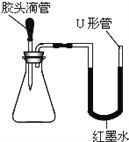
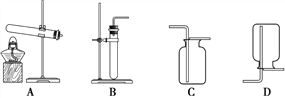
小明用白色粉末和水反应制取并收集产生的气体时,应选用的装置是_____(填序号)。 经检验该气体是氧气。
实验2:检验反应后溶液中的溶质成分
(猜想假设)小明猜想:Na2CO3 小刚猜想:Na2CO3和NaOH
(进行实验)小明取实验1反应后的溶液于试管中,滴加1%的CaCl2溶液,观察到有白色沉淀生成,认为自己的猜想正确。
(表达交流)①小刚对小明的实验方案提出质疑,他的理由是_________________。
②为了证明小明的猜想是否正确,你的实验方案是________________。
(3)反思拓展
根据上述探究可知,保存该白色粉末时应注意___________。