题目内容
【题目】为了对氯化钾样品(含少量的KNO3)进行分析,甲、乙、丙三位同学分别进行实验,他们的实验数据如下表,清仔细观察和分析数据,回答下列问题:
甲 | 乙 | 丙 | |
所取固体样品的质量/g | 20 | 10 | 10 |
加入AgNO3溶液的质最/g | 100 | 100 | 150 |
反应后所得沉淀质量/g | 14.35 | 14.35 | 14.35 |
(1)三位同学中,哪一位同学所用的氯化钾与硝酸银刚好相互完全反应____ (填写编号)。
(2)样品中氯化钾的质量分数是多少? ______
(3)三位同学分别把反应后的溶液过滤(操作中的损失可忽略不计),哪一位同学所得的滤液是只含有一种溶质的溶液________?此溶液中溶质的质量分数是多少? ______
【答案】(1)乙;(2)74.5%;(3)乙;13.2%
【解析】
(1)甲、乙两组数据对照,说明甲中固体过量,硝酸银溶液完全反应;乙、丙两组数据对照,说明丙中硝酸银溶液过量,固体完全反应;以上分析说明乙中固体于硝酸银溶液恰好完全反应。故填:乙;
(2)解:设10g样品中氯化钾质量为x,消耗硝酸银质量为y,生成硝酸钾质量为z,
![]()
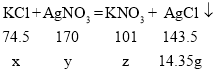
![]() ,x=7.45g
,x=7.45g
![]() ,y=17g
,y=17g
![]() ,z =10.1g
,z =10.1g
样品中氯化钾的质量分数是:![]() ;
;
(3)甲同学得到的溶液中,含有的溶质是硝酸钾和氯化钾,硝酸钾包括样品中的硝酸钾和反应生成的硝酸钾,氯化钾是过量剩余的氯化钾;
丙同学得到的溶液中,含有硝酸钾和硝酸银,硝酸钾包括样品中的硝酸钾和反应生成的硝酸钾,硝酸银是过量剩余的硝酸银;
乙同学得到的溶液中,只含有硝酸钾,包括样品中的硝酸钾和反应生成的硝酸钾;
反应后所得溶液质量=![]()
反应后所得溶液溶质质量分数=![]()
答:乙同学所得滤液只含一种溶质,质量分数为13.2%。

练习册系列答案
 名校课堂系列答案
名校课堂系列答案
相关题目