题目内容
【题目】如图是某胃药标签上的部分内容,孔明中学化学兴趣小组欲测定该药品中碳酸氢钠(NaHCO3)的质量分数,取20片该药品研碎放入烧杯中,再向烧杯中滴加稀盐酸至恰好完全反应(杂质不溶于水,也不参加反应),共消耗稀盐酸46. 0g,测得反应后烧杯内物质的总质量为51.6g。请计算:

(1)反应共生成气体的质量为_____。
(2)反应后所得溶液中溶质的质量分数_____。
【答案】4.4g 11.7%
【解析】
(1)20片该药品质量=![]() ,根据质量守恒定律可知,反应共生成气体的质量=10g+46g-51.6g=4.4g;
,根据质量守恒定律可知,反应共生成气体的质量=10g+46g-51.6g=4.4g;
(2)设生成4.4g二氧化碳需要碳酸氢钠的质量为x,同时生成氯化钠的质量为y。
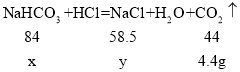
![]() ,x=8.4g
,x=8.4g
![]() ,y=5.85g;
,y=5.85g;
反应后所得溶液中溶质的质量分数=![]()
答:反应后所得溶液中溶质的质量分数为11.7%。

练习册系列答案
相关题目