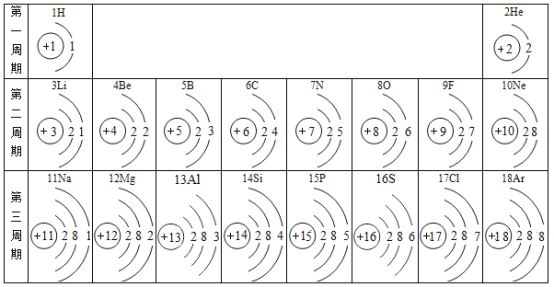
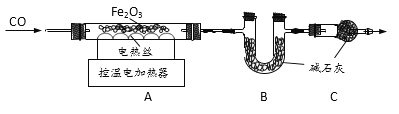
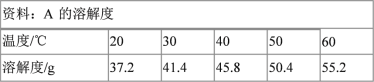题目内容
【题目】请结合下图回答问题:

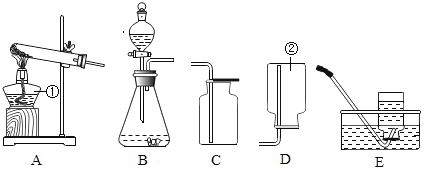
(1)仪器名称:①______,②_______。
(2)高锰酸钾制O2的化学方程式___,选择___装置收集可得到纯净O2。
(3)实验室制取CO2的化学方程式____,选择C相对于B装置的优点是___,可用D装置收集CO2,理由是___。
(4)实验室可用次氯酸钠粉末和浓盐酸在常温下反应制取氯气,氯气的密度比空气大、有毒。据此你认为实验室制取氯气时,最好选用的发生装置是 _____,如果用甲装置收集氯气,气体应从____(填“a”或“b”)口进,用乙装置收集氯气,由图可知氯气具有____的性质。(只要求答一点)。

【答案】铁架台 分液漏斗 2KMnO4![]() K2MnO4+MnO2+O2↑ E CaCO3+2HCl=CaCl2+H2O+CO2 ↑ 控制反应的发生与停止 二氧化碳的密度比空气大 B b 可溶于水
K2MnO4+MnO2+O2↑ E CaCO3+2HCl=CaCl2+H2O+CO2 ↑ 控制反应的发生与停止 二氧化碳的密度比空气大 B b 可溶于水
【解析】
(1)仪器名称:①铁架台,②分液漏斗;
(2)高锰酸钾在加热条件下分解生成锰酸钾、二氧化锰、氧气,化学方程式2KMnO4![]() K2MnO4+MnO2+O2↑,排水法收集气体较纯,装置为E;
K2MnO4+MnO2+O2↑,排水法收集气体较纯,装置为E;
(3)实验室制取CO2的原理是碳酸钙和盐酸反应生成二氧化碳、氯化钙、水,化学方程式CaCO3+2HCl=CaCl2+H2O+CO2 ↑,选择C相对于B装置的优点是控制反应的发生和停止,关闭弹簧夹,U型管内气体增多,压强变大,在压力的作用下,U型管内右边液面下降,当液面下降到隔板下边时,固体反应物与液体分离,反应停止;反之,打开弹簧夹,反应开始。可用D装置收集CO2,理由是二氧化碳的密度比空气的大,能溶于水;
(4)实验室可用次氯酸钠粉末和浓盐酸在常温下反应制取氯气,据此实验室制取氯气时,最好选用的发生装置是固-液常温型B,如果用甲装置收集氯气,氯气的密度比空气的大,气体应从b口进,用乙装置收集氯气,需要将氯气和水用植物油隔开,可知氯气具有可溶于水的性质。

 口算题卡加应用题集训系列答案
口算题卡加应用题集训系列答案