题目内容
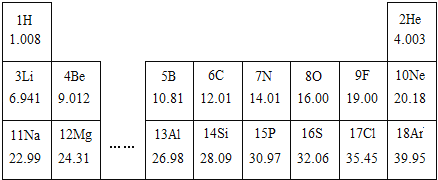
【题目】(1)下表为元素周期表中部分元素的相关信息,请利用下表回答相关问题.
①下列各组具有相似化学性质的元素是________(填字母序号)
a.Na、Cl b.O、S c.F、Cl d.Cl、Ar
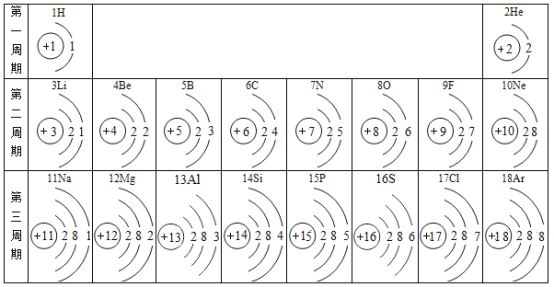
②氖原子(Ne)的核内质子数为____,写出一条第三周期元素原子的核外电子排布规律_____。
③11号元素的原子在化学反应中比较容易________(填“得到”或“失去”)电子,由它和6号8号元素形成化合物的化学式是________.
(2)用微粒的观点解释下列问题,将对应的字母序号填入空格内。
a.分子结构不同 b.微粒间隔变大
c.微粒在不断运动 d.原子的排列方式不同
①经过花园能够闻到花香,这是因为______________。
②用水银温度计测量体温,温度升高,温度计示数变大的原因是________。
③一氧化碳和二氧化碳的组成元素相同,它们的化学性质不同的原因是_______。
④金刚石和石墨都是碳单质,它们的物理性质差别很大的原因是________。
【答案】bc 10 质子数从左向右依次递增或最外层电子数从左向右依次递增 失去 Na2CO3 c b a d
【解析】
(1)①具有相似化学性质的元素则最外层电子数相同,在元素周期表中位于同一族。
a. Na和Cl不是同一族,不具有相似的化学性质;
b. O和S是同一族,具有相似的化学性质;
c. F和Cl是同一族,具有相似的化学性质;
d. Cl和Ar不是同一族,不具有相似的化学性质;故填:bc;
②氖原子(Ne)的原子序数为10,则核内质子数为10;在元素周期表中,处于同一周期的元素的原子,核外电子层数相同;同一周期元素的原子,从左至右最外层电子数依次增大。第三周期元素原子的核外电子排布规律:质子数从左向右依次递增或最外层电子数从左向右依次递增;
③11号元素是钠元素,钠原子的最外层有1个电子,在化学反应中易失去最外层电子;6号元素是碳元素,8号是氧元素,三者组成的化合物是碳酸钠,化学式为:Na2CO3;
(2)①经过花园能够闻到花香,这是因为微粒在不断运动。故选c;
②用水银温度计测量体温,温度升高,温度计示数变大的原因是微粒间隔变大。故选b;
③一氧化碳和二氧化碳的组成元素相同,它们的化学性质不同的原因是分子结构不同。故选a;
④金刚石和石墨都是碳单质,它们的物理性质差别很大的原因是原子的排列方式不同。故选d。

 时刻准备着暑假作业原子能出版社系列答案
时刻准备着暑假作业原子能出版社系列答案【题目】实验室常用的制取二氧化碳气体的研究如下:
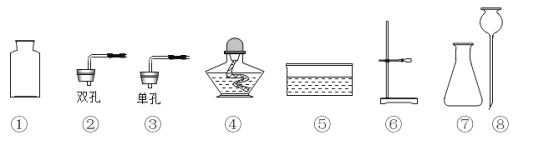
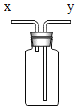
(1)仪器问题:制取二氧化碳的发生装置,除了用到⑦号仪器外,还需选择的仪器是________(填序号)。收集二氧化碳,用如图装置收集时,空气从_____(选填“x”或“y”)端排出。
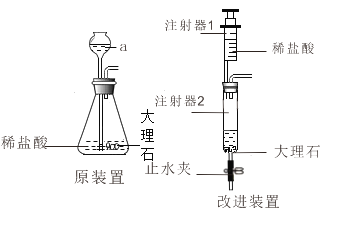
(2)装置改进:
仪器a的名称是_______;使用其优点为__________;改进装置的优点是_________________(写一条即可)。
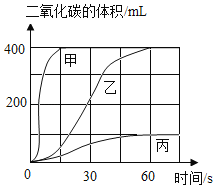
(3)选用药品:按下表进行实验,取等质量的大理石加入足量酸中(杂质不与酸反应),产生二氧化碳体积随时间变化曲线如图所示:
实验编号 | 药品 |
Ⅰ | 块状大理石、10%H2SO4溶液 |
Ⅱ | 块状大理石、7%HCl溶液 |
Ⅲ | 大理石粉末、7%HCl溶液 |
图中丙对应实验_____(选填“I”“Ⅱ”或“Ⅲ”)。确定用乙对应的药品制备并收集二氧化碳,相应的化学方程式是________;不用甲对应的药品,理由是________。