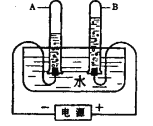
题目内容
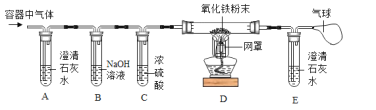
【题目】A~K是初中化学常见物质,它们之间的转化关系如图所示(反应条件已略去).其中B是红棕色固体,G为红色固体,A、E为气体:
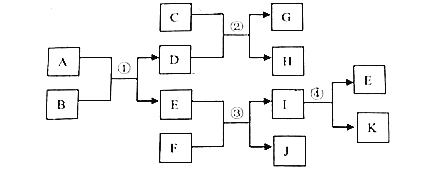
请回答下列问题
(1)请写出以下物质的化学式:F________;G__________.
(2)化合物H中所含金属元素呈现的化合价为_________。
(3)反应①的化学方程式为______________________________。
(4)反应④的化学方程式为_______________________________。
【答案】Ca(OH)2 Cu +2 Fe2O3+3CO![]() 2Fe+3CO2 CaCO3
2Fe+3CO2 CaCO3![]() CaO+CO2↑
CaO+CO2↑
【解析】
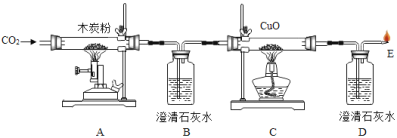
B是红棕色固体,则B是氧化铁。G为红色固体,G可以是铜。A、E为气体,且A能与氧化铁反应,则A是一氧化碳,E是二氧化碳,D是被还原的铁。铁能与硫酸铜溶液反应,生成铜和硫酸亚铁,则C是硫酸铜,H是硫酸亚铁;二氧化碳能与氢氧化钙溶液反应生成碳酸钙沉淀和水,碳酸钙能分解生成氧化钙和二氧化碳,故F是氢氧化钙,J是水,I是碳酸钙,K是氧化钙。
(1) 由分析可知F为氢氧化钙,G为铜。故F的化学式为Ca(OH)2;G为Cu;
(2)化合物H为硫酸亚铁,硫酸亚铁中硫酸根显-2价,故所含金属元素的化合价为0-(-2)=+2;
(3)反应①是氧化铁与一氧化碳在高温的条件下反应,生成铁和二氧化碳。反应的化学方程式为:Fe2O3+3CO![]() 2Fe+3CO2;
2Fe+3CO2;
(4)反应④是碳酸钙在高温的条件下分解生成氧化钙和二氧化碳,反应的化学方程式为:CaCO3![]() CaO+CO2↑。
CaO+CO2↑。

【题目】(1)下表是生活饮用水国家标准的部分内容。
生活饮用水水质常规检验项目及限值(部分)
项目 | 限值 |
色度 | 不超过15度,并不得呈现其他异色 |
浑浊度 | 不超过1度,特殊情况下不超过5度 |
pH | 6.5~8.5 |
总硬度(以CaCO3计) | 450mg/L |
铝 | 0.2mg/L |
铁 | 0.3mg/L |
硫酸盐 | 250mg/L |
①上表中“铝”指的是_______(选填“单质”“元素”或“原子”)。
②生活中硬水软化的方法是___________。
③Cl2、ClO2均可作自来水消毒剂,其中氯元素的化合价分别是____________。
④1L合格的生活饮用水中,均以CaCO3计算硬度,则钙元素的含量不超过_____mg/L。
⑤实验室用上述水样通电分解,产生氢气和氧气的体积比约为______;反应的化学方程式为______。
(2)元素周期表是学习化学的重要工具。下面是元素周期表中1~18号元素原子核外电子排布:
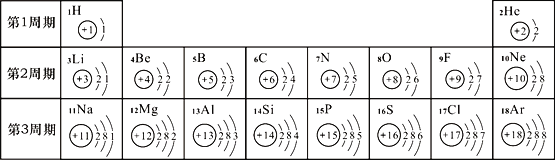
请回答下列问题:
①第17号元素属于______元素(填“金属”或“非金属”),其次外层电子数为______。
②元素的化学性质与原子结构中的_____数关系密切;在同一族中,各元素的原子结构呈现的规律有____(任写一点)。
③地壳中含量最多的金属元素与含量最多的非金属元素组成的化合物为____________。第16号元素在化学反应中容易形成________(填离子符号),该元素的单质在氧气中燃烧的现象是_______________。