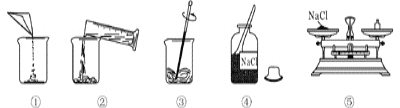
题目内容
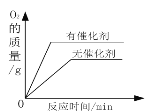
【题目】某同学取一定质量的氯酸钾和二氧化锰加热,记录产生氧气的质量与反应时间的关系如图所示,请回答下列问题:
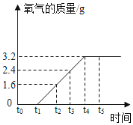
(1)t2时,试管内固体的成分是__________
(2)混合物中原氯酸钾的质量为_______?(写出过程,计算结果保留一位有效数字)
【答案】KClO3 、KCl 、MnO2 8.2g(详见解析)
【解析】
(1)根据图中信息可知:t2后氧气的质量不断增加,说明t2时,反应正在进行中,氯酸钾加热时在二氧化锰催化作用下分解生成氯化钾和氧气,氧气逸出,t2时,试管内固体的成分是未反应的氯酸钾,反应生成的氯化钾和用作催化剂的二氧化锰,即KClO3、KCl、MnO2;
(2)根据图中信息可知:混合物中原氯酸钾完全分解后产生的氧气质量为3.2g。
设:混合物中原氯酸钾的质量为x。
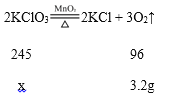
![]() 解得x=8.2g。
解得x=8.2g。
答:氯酸钾的质量为8.2g。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
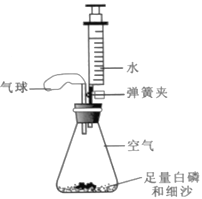
小学生10分钟应用题系列答案【题目】如图将纸花放入集气瓶中,表格中下列说法不正确的是 ( )
纸花 | 集气瓶中盛放的物质 | 集气瓶中纸花颜色的变化 | |
A | 紫色石蕊浸泡后,晾干的纸花 | 二氧化碳 | 纸花仍为紫色 |
B | 紫色石蕊浸泡后的湿纸花 | 二氧化碳 | 纸花由紫色变为红色 |
C | 紫色石蕊浸泡后的湿纸花 | 少量醋酸 | 纸花由紫色变为红色 |
D | 酚酞溶液浸泡后的湿纸花 | 少量浓氨水 | 纸花由红色变为无色 |
A. A B. B C. C D. D
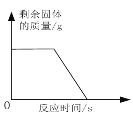
【题目】化学兴趣小组为测定一批石灰石样品中碳酸钙的质量分数,取用20g石灰石样品,进行高温煅烧(样品中除碳酸钙外,其余成分高温不分解。碳酸钙分解的化学方程式为CaCO3 == CaO + CO2↑),不同时间测得剩余固体的质量如下表所示:
煅烧的时间(min) | 剩余固体的质量(g) |
2 | 17.8 |
4 | 13.4 |
6 | 12.3 |
8 | 12.3 |
(1)完全反应后生成二氧化碳的质量_____________。
(2)求石灰石样品中碳酸钙的质量分数_______
【题目】某化学兴趣小组在学习催化剂的概念后,想研究不同的氧化物能否在氯酸钾制取氧气实验中起催化作用,进行了以下实验:
实验编号 | KClO3/g | 氧化物 | 产生气体的体积(mL) | 耗时(s) |
1 | 0.6 | / | 9.8 | 480 |
2 | 0.6 | 0.2g二氧化锰 | 67 | 36.5 |
3 | 0.6 | 0.2g氧化铜 | 67 | 89.5 |
⑴写出实验2反应的化学方程式____________________。
⑵为证明氧化铜是该反应的催化剂,同学们又完成了以下的实验:
Ⅰ.在实验3反应后的混合物中加足量的水溶解,过滤,将滤渣洗涤并干燥,用电子天平称量,质量为0.2g。
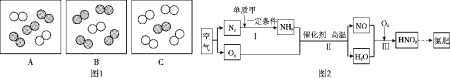
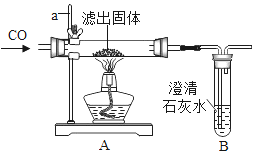
Ⅱ.将过量的CO通入滤出的固体,按如图进行实验:仪器a的名称_________________。
⑶甲同学的实验报告如下:
装置 | 现象 | 实验结论 |
A | 黑色固体全部变红 | 生成了铜,反应方程式________________ |
B | 石灰水变浑浊 | 产生了二氧化碳 |
Ⅲ.该实验装置存在的缺陷是______________;当出现______现象时,证明反应已经开始。
⑷以上实验证明氧化铜在反应前后质量和化学性质都没改变,能作为氯酸钾受热分解的催化剂。两种氧化物相比,________的催化效果更好。