题目内容
【题目】燃烧是人类最早利用的化学反应之一,请据图回答:
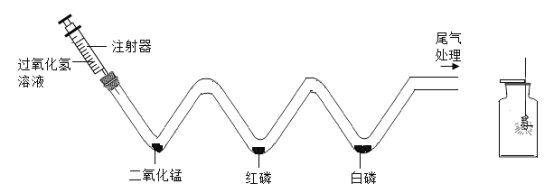
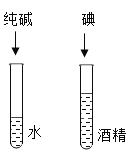
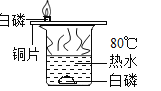
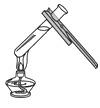
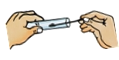
(1)将注射器中的溶液缓缓推入 V 形管,有关反应的化学方程式为____________;用80℃的热水加热盛有红磷和白磷的 W 形管时,发现白磷燃烧而红磷不燃烧,由此可说明燃烧需要的条件是_________。
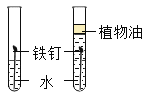
(2)铁丝在氧气中燃烧的现象为__________。该实验装置存在明显不足,改进措施是__________。
(3)室内起火时,若打开门窗,火会烧得更旺的原因_________。
(4)列举一种你所知道的清洁能源____________。
【答案】2H2O2![]() 2H2O+O2↑ 温度达到可燃物的着火点 剧烈燃烧,火星四射,放出大量的热,生成黑色固体 在集气瓶底部放少量的水 形成对流,增大了氧气的含量 太阳能(合理均可)
2H2O+O2↑ 温度达到可燃物的着火点 剧烈燃烧,火星四射,放出大量的热,生成黑色固体 在集气瓶底部放少量的水 形成对流,增大了氧气的含量 太阳能(合理均可)
【解析】
(1)过氧化氢在二氧化锰的催化作用下分解为水和氧气,反应的化学方程式为2H2O2![]() 2H2O+O2↑;用80℃的热水加热盛有红磷和白磷的W形管时,发现白磷燃烧而红磷不燃烧,二者都是可燃物,都接触氧气,但是由于着火点不同,所以现象不同,由此可说明燃烧需要温度达到可燃物着火点。
2H2O+O2↑;用80℃的热水加热盛有红磷和白磷的W形管时,发现白磷燃烧而红磷不燃烧,二者都是可燃物,都接触氧气,但是由于着火点不同,所以现象不同,由此可说明燃烧需要温度达到可燃物着火点。
(2)铁丝在氧气中燃烧的现象:剧烈燃烧,火星四射,放出大量的热,生成黑色固体。该实验装置中没有在集气瓶底部放少量的水,溅落的热的固体容易炸裂集气瓶。
(3)室内起火时,若打开门窗,火会烧得更旺,是因为形成对流,增大了氧气的含量。
(4)太阳能、风能、氢能等都是常见的清洁能源。

【题目】兴趣小组的同学寒假期间参观故宫时对篆刻艺术产生了兴趣。他们查阅资料后尝试自行制作“化学印章”,并对印记效果进行了研究。

(查阅资料)篆刻中,印记白底红字称“朱文”,红底白字称“白文”。
实验1:初步实验。
用NaOH溶液浸泡白纸并晾干。用酚酞溶液作“化学印泥”。用不与酸碱反应的印章蘸取印泥,印在碱性白纸上产生的印记效果如下:
实验编号 | 1-1 | 1-2 | 1-3 |
NaOH溶液的浓度 | 4 g/L | 6 g/L | 20 g/L |
酚酞溶液的浓度 | 2 g/L | 6 g/L | 3 g/L |
印记颜色 | 浅红色 | 红色 | 红色 |
(1)酚酞“印泥”能在碱性白纸上留下红色印记,原因是__________。
(2)根据初步实验,可能影响印记颜色深浅的因素有__________。
实验2:深入探究。
取4 g/L NaOH溶液浸泡白纸并晾干,用不同浓度的酚酞做“化学印泥”继续实验。现象如下:
实验编号 | 2-1 | 2-2 | 2-3 |
NaOH溶液的浓度 | 4 g/L | 4 g/L | 4 g/L |
酚酞溶液的浓度 | 1g/L | 3 g/L | 5 g/L |
印记颜色 | 浅红色 | 浅红色 | 红色 |
(3)实验2的目的是_________。
(4)实验1和2中,支持猜想“NaOH溶液浓度会影响印记颜色”的实验是________ (填实验编号)。
(5)若所用印章文字是向外凸的,碱性纸上留下的印记效果是_______(填“朱文”或“白文”)。
(6)有同学希望印记产生“白文”效果,以下不能达到目的的做法是_________(填字母序号)。
A.用文字向外凸的印章,用 NaOH 溶液作“印泥”,白纸用酚酞溶液浸泡
B.用文字向外凸的印章,用稀盐酸做“印泥”,白纸用混有NaOH的酚酞溶液浸泡
C.用文字向内凹的印章,印泥和白纸同实验2中
【题目】芯片是内含集成电路的硅片,如图是硅元素在元素周期表中的相关信息,下列说法不正确的是
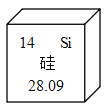
A.硅元素的原子序数为14
B.硅原子核内中子数可能为14
C.硅的相对原子质量为28.09
D.硅元素属于金属元素
【题目】我国约在南北朝时就开始冶炼黄铜,黄铜是铜和锌的合金(Cu-Zn) ,它可用来制造电器零件及日用品。将30g稀盐酸分三次加入到10g 黄铜样品粉末中(不考虑黄铜中的其他杂质),每次充分反应后,测定本次生成氢气的质量,实验数据见下表:
次数 | 第一次 | 第二次 | 第三次 |
加入稀盐酸的质量(g) | 10 | 10 | 10 |
本次生成氢气的质量(g) | 0.04 | m | 0.02 |
请回答:
(1)工业上常用铜作电缆的内芯,是利用铜具有良好的____________性。
(2) m=____________。
(3)所用稀盐酸的溶质质量分数___________? (结果精确到0.1)