题目内容
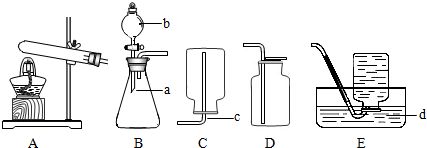
“化学反应条件的控制是实验的灵魂”。某校化学兴趣小组在老师指导下,进行了“影响双氧水(过氧化氢溶液)分解因素”的探究实验。下表是该化学兴趣小组研究影响过氧化氢(H2O2)分解速率的因素时采集的一组数据:
用10mL H2O2溶液制取150mL氧气所需的时间(秒)
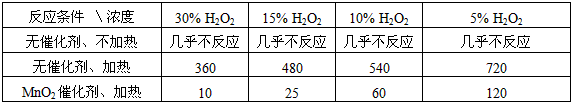
请你分析回答:
①该研究小组在设计方案时。考虑了浓度、__________、_________等因素对过氧化氢分解速率的影响。
②从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对分解速率有何影响?_____________。
①该研究小组在设计方案时。考虑了浓度、__________、_________等因素对过氧化氢分解速率的影响。
②从上述影响过氧化氢分解速率的因素中任选一个,说明该因素对分解速率有何影响?_____________。
① 温度;催化剂
② 浓度越高,过氧化氢的分解速率越快(或温度越高,过氧化氢的分解速率越快;使用催化剂,过氧化氢的分解速率越快)
② 浓度越高,过氧化氢的分解速率越快(或温度越高,过氧化氢的分解速率越快;使用催化剂,过氧化氢的分解速率越快)

练习册系列答案
相关题目
 “化学反应条件的控制是实验灵魂”.某校化学兴趣小组在老师指导下,进行了“影响过氧化氢溶液分解因素”的实验.请你帮助回答下列问题.
“化学反应条件的控制是实验灵魂”.某校化学兴趣小组在老师指导下,进行了“影响过氧化氢溶液分解因素”的实验.请你帮助回答下列问题.