题目内容
【题目】含氧原子个数约为6.02×1023的物质是
A. 1molH2O2 B. 0.5molSO2 C. 4.4gCO2 D. 180mL H2O
【答案】B
【解析】A、1mol任何物质中含有6.02×1023个分子,一个H2O2分子含有2个氧原子,故1molH2O2中有1mol×2×6.02×1023个=12.04×1023个氧原子,故选项错误;
B、1mol任何物质中含有6.02×1023个分子,一个SO2分子含有2个氧原子,故0.5molSO2中有0.5mol×2×6.02×1023个=6.02×1023个氧原子,故选项正确;
C、二氧化碳的摩尔质量是44g/mol,44g二氧化碳的物质的量为![]() =1mol;1mol任何物质中含有6.02×1023个分子,一个CO2分子含有2个氧原子,故1molCO2中有1mol×2×6.02×1023个=12.04×1023个氧原子,故选项错误;
=1mol;1mol任何物质中含有6.02×1023个分子,一个CO2分子含有2个氧原子,故1molCO2中有1mol×2×6.02×1023个=12.04×1023个氧原子,故选项错误;
D、180mLH2O没有指出状态,其质量无法确定,故选项错误。

 活力课时同步练习册系列答案
活力课时同步练习册系列答案【题目】如图所示为实验室中常见的气体制备、净化、收集和性质实验的部分仪器。试根据题目要求,回答下列问题(所选仪器装置,填写序号字母):
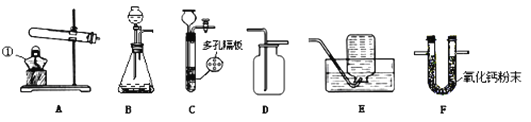
(Ⅰ)写出仪器①的名称:①_____________ 。
(Ⅱ)若用双氧水与二氧化锰为原料制取并收集一瓶干燥的氧气。则应选的气体发生装置为___,反应的化学方程式为______________;应选的气体干燥装置为________。
(Ⅲ)科技小组的同学对实验室制取CO2的实验条件展开了探究,探究实验如下表:
实验编号 | 反应物 | 反应现象 | |
① | 取mg块状大理石 | 足量的溶质质量分数为5%的盐酸 | 产生气泡较慢 |
② | 取mg大理石粉末 | 足量的溶质质量分数为5%的盐酸 | 产生气泡快 |
③ | 取mg块状大理石 | 足量的溶质质量分数为10%的盐酸 | 产生气泡较快 |
④ | 取mg大理石粉末 | 足量的溶质质量分数为10%的盐酸 | 产生气泡很快 |
实验结论:影响大理石和盐酸反应快慢的因素有______ 、________。
【题目】为探究酸的化学性质,进行如下实验:

① 甲实验没有观察到明显现象,乙实验现象是______________
② 将反应后甲乙两试管中的溶液部分倒入烧杯中,没有观察到明显现象.
由此猜想反应后乙试管中溶液的溶质:
a.NaCl、 HCl .__________________
③ 为了验证猜想a,某同学对乙试管中剩余溶液,设计了如下实验方案。
方案编号 | 实验操作 | 实验现象 | 结论 |
方案1 | 取样于试管中,滴加紫色石蕊试液 | __________ | 猜想a成立 |
方案2 | 取样于试管中,滴加硝酸银溶液 | 产生白色沉淀 |
Ⅰ.方案2不合理的理由是_________________(用化学方程式表示)。
Ⅱ.下列物质代替石蕊试液,也可以达到验证目的,其中不正确的是_____(填序号)。
A.铁粉 B.碳酸钠粉末 C.氧化铜粉末 D.氢氧化钠
④ 利用酸的性质测定锌铜混合物中铜的质量分数。取10g样品置于烧杯中,加入一定质量的稀硫酸。所加稀硫酸与生成气体的质量关系如下图所示。

Ⅰ.氢气的物质的量是______________mol 。
Ⅱ.求该样品中铜的质量分数。(利用化学方程式计算)______________
