题目内容
【题目】化学是一门以实验为基础的学科,请结合图示回答问题:
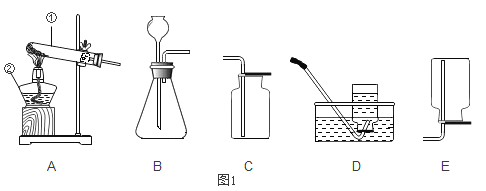
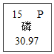
(1)写出如图1标号仪器的名称:①_____,②_____。
(2)若用高锰酸钾制氧气,主要操作步骤有:①从水槽中取出导管;②检查装置的气密性;③停止加热;④收集气体;⑤加热;⑥加入药品。请写出正确的操作顺序_____ (填序号),反应的化学方程式为_____;现准备收集一瓶氧气供铁丝燃烧的实验使用,最好选择的收集装置是_____(填字母,下同)。
(3)实验室制取二氧化碳气体可选用的发生装置为_____,收集装置是_____。
(4)将生成的二氧化碳通入澄清石灰水中,没有观察到明显现象。某同学认为该二氧化碳气体中混有氯化氢气体。并设计了如图2所示实验装置检验该二氧化碳中是否含有氯化氢气体。
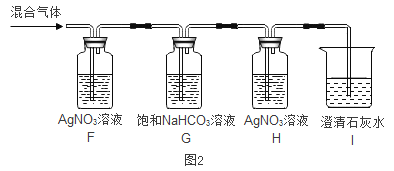
①若证明收集到的气体中含有氯化氢气体,观察到的现象为_____。
②设置H装置的目的是_____。
【答案】试管 酒精灯 ②⑥⑤④①③ ![]() D B C F中产生白色沉淀 检验氯化氢气体是否除尽
D B C F中产生白色沉淀 检验氯化氢气体是否除尽
【解析】
高锰酸钾加热生成锰酸钾、二氧化锰和氧气,碳酸钙与稀盐酸在常温下反应生成氯化钙、水和二氧化碳,硝酸银和盐酸反应生成氯化银和硝酸。
(1)仪器名称分别①是试管,②是酒精灯。
(2)实验室用高锰酸钾制氧气的主要操作步骤是检查装置的气密性、加入药品、加热、收集气体、从水槽中取出导管、停止加热,故顺序为②⑥⑤④①③。高锰酸钾受热分解生成锰酸钾、二氧化锰和氧气,故制取氧气的化学方程式为![]() 。做铁丝在氧气中燃烧的实验时,为防止铁丝燃烧的高温熔融物溅落瓶底使集气瓶炸裂,应在盛有氧气的集气瓶中装入少量的水,故最好选择排水法收集氧气,氧气比较纯净,故选D。
。做铁丝在氧气中燃烧的实验时,为防止铁丝燃烧的高温熔融物溅落瓶底使集气瓶炸裂,应在盛有氧气的集气瓶中装入少量的水,故最好选择排水法收集氧气,氧气比较纯净,故选D。
(3) 实验室制取二氧化碳气体的反应原理是碳酸钙与稀盐酸在常温下反应生成氯化钙、水和二氧化碳,反应物是固体与液体,反应在常温下进行,故选用的发生装置是B,二氧化碳的密度大于空气,能溶于水且能与水反应,故选用的收集装置是C。
(4)①若收集到的气体中含有氯化氢,可观察到F中硝酸银会和氯化氢反应生成氯化银白色沉淀,故当F装置中出现白色沉淀时,可证明含有氯化氢气体。
②硝酸银会和氯化氢反应生成氯化银白色沉淀,故设置H装置的目的是检验氯化氢气体是否除尽。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
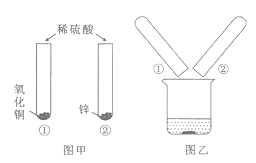
小学生10分钟应用题系列答案【题目】某化学兴趣小组的同学为了探究“复分解反应发生的条件”,做了如图两个实验:
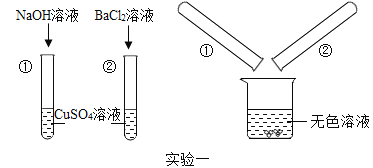
(实验一):把试管①②中静置后的上层清液倒入洁净的烧杯中,最后只得到蓝色沉淀和无色溶液。
(1)写出混合后得到蓝色沉淀一定发生反应的化学方程式_____________。
(2)混合后所得无色溶液中一定含有的溶质是________________(填化学式,下同)可能含有的溶质是_______________。
(实验二):按照下列组合继续验证复分解反应发生的条件:
组合序号 | ① | ② | ③ |
组合的溶液 | H2SO4NaOH | H2SO4NaCl | H2SO4Na2CO3 |
(3)在组合①、②、③中,组合____________无明显现象,但它们的实质不同,为了证明实质不同,小夕在实验过程中使用了酚酞试液。
(4)实验结束后把3个组合反应后的溶液混合,混合后溶液也显无色。混合后所得溶液中溶质(除酚酞外)的组成可能有____________种情况(填数字)。
(结论)
(5)复分解反应发生的条件是:生成物中有______________。
【题目】下列实验方法一定能达到实验目的的是
选项 | 实验目的 | 实验方法 |
A | 检验一瓶气体是否为 | 将燃着的木条伸入瓶中 |
B | 鉴别 | 分别点燃,在火焰上方罩一干冷烧杯 |
C | 鉴别石灰水和 | 加入适量的稀盐酸 |
D | 比较Zn、Cu、Ag的金属活动性 | 将Zn和Ag分别放入 |
A. A B. B C. C D. D