题目内容
【题目】用化学方程式解释下列事实,并注明反应的基本类型。
(1)工业上用高温煅烧石灰石的方法制生石灰____ 、
(2)生石灰做干燥剂______ 、
(3)用熟石灰改良硫酸型酸雨造成的土壤酸化___ 、
【答案】CaCO3![]() CaO+ CO2↑、分解反应 CaO+H2O=Ca(OH)2、化合反应 Ca(OH)2+H2SO4= CaSO4+2H2O 、复分解反应
CaO+ CO2↑、分解反应 CaO+H2O=Ca(OH)2、化合反应 Ca(OH)2+H2SO4= CaSO4+2H2O 、复分解反应
【解析】
(1)石灰石主要成分是碳酸钙,工业上用高温煅烧石灰石的方法制生石灰,反应的化学方程式为:CaCO3![]() CaO+ CO2↑,一种物质发生化学反应生成两种或两种以上物质的反应是分解反应。
CaO+ CO2↑,一种物质发生化学反应生成两种或两种以上物质的反应是分解反应。
(2)生石灰是氧化钙的俗称,能与水反应,反应的化学方程式为:CaO+H2O=Ca(OH)2,两种或两种以上的物质发生化学反应生成一种物质的反应是化合反应。
(3)熟石灰是氢氧化钙,硫酸型酸雨中含有硫酸,用熟石灰改良硫酸型酸雨造成的土壤酸化的化学方程式为:Ca(OH)2+H2SO4= CaSO4+2H2O,由两种化合物互相交换成分生成另外两种化合物的反应是复分解反应。

【题目】2009年邵阳市九年级化学实验操作技能考试中,小聪同学抽到的试题是“探究酸和碱之间的中和反应“。他向盛有氢氧化钠溶液的烧杯中缓慢滴加稀盐酸,一会儿后,想起忘记加指示剂了,便补加几滴无色酚酞溶液,搅拌,观察到溶液不变色,于是他得出“酸碱恰好完全中和”的结论。
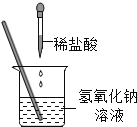
(1)该中和反应的化学方程式是_____;
(2)老师给予小聪的评定是结论不准确。请你帮小聪分析老师的理由是:_____
(3)请你另外设计一个实验,探究小聪实验后烧杯中的溶液是否“恰好完全中和”。
填写下表:
实验步骤 | 实验现象 | 实验结论 |
_____ | _____ | _____ |
_____ | _____ |
【题目】实验室有一瓶标签残缺并且瓶盖没有完全密封的无色溶液(如图),化学小组的同学询问老师后知道是NaCl、NaOH、Na2CO3、NaHCO3中的某一种溶液。为确认原瓶中是何种溶质的溶液并判断其是否变质化学小组的同学进行了如下的探究活动:
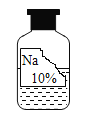
(做出猜想)
猜想a:原溶液的溶质是NaCl 猜想b:原溶液的溶质是NaOH
猜想c:原溶液的溶质是Na2CO3 猜想d:原溶液的溶质是 NaHCO3
(查阅资料)
常温下,有关物质的相关信息如表
物质 | NaCl | NaOH | Na2CO3 | NaHCO3 |
常温下的溶解度/g | 36 | 109 | 21.5 | 9.6 |
常温下稀溶液的pH | 7 | 13 | 11 | 9 |
从物质的相关信息可知原溶液的溶质一定不是NaHCO3,因为_____。
(进行实验)
(1)取少量样品测得溶液的pH大于7,则原溶液的溶质肯定不是_____。
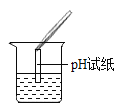
(2)下列检测溶液pH的实验操作方法中,正确的是_____(填字母序号)。
A 将pH试纸直接插入待测液中
B 将pH试纸放在表面皿上,用干净的玻璃棒蘸取待测液滴在pH试纸
C 将pH试纸湿润后放在表面皿上,用千净的玻璃棒蘸取待测液滴在pH试纸上
D 读数时将pH试纸呈现的颜色与标准比色卡对照
(3)同学们另取样品又进行了如下实验,实验过程如图:

①生成白色沉淀A的化学反应方程式_____。
②通过实验可以判断样品无色溶液中含有的溶质是_____和_____(填化学式)
(得出结论)
实验完成后,最终得到的结论:原瓶溶液中的溶质是_____,且已变质。