题目内容
【题目】某研究性学习小组从含有Hg(NO3)2、Cu(NO3)2的实验室废液中回收金属汞和铜,设计的实验方案如图所示:
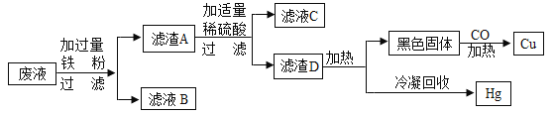
(1)操作Ⅰ所用的玻璃仪器有烧杯、玻璃棒、__________。
(2)加过量铁粉的目的是________。写出加入适量稀硫酸反应的化学方程式________。判断加入稀硫酸“适量”的实验现象是________。
(3)黑色固体转化为Cu的化学方程式是_________;_________,(填化学式)发生了还原反应。
(4)为防止有毒的汞蒸气扩散污染环境,冷凝回收汞的操作应________(填序号) 。
①用导管通入装有水的大试管;
②用导管通入带胶塞的锥形瓶;
③通入干冷烧杯;
④通入密闭并有冷凝功能的装置。
【答案】)漏斗 使废液的Hg(NO3)2、Cu(NO3)2中Hg、Cu完全被置换出 Fe+H2SO4=FeSO4+H2↑ 溶液中恰好没有气泡产生 CuO+CO![]() Cu+CO2 CuO ①④
Cu+CO2 CuO ①④
【解析】
(1)由图可知,操作I均是将固体与液体进行分离,故操作为过滤。过滤时用到的仪器有:铁架台、烧杯、漏斗、玻璃棒。故填:漏斗。
(2)根据金属活动性顺序,Fe排在Cu、Hg之前,加入过量铁粉的目的是使废液的Hg(NO3)2、Cu(NO3)2中Hg、Cu 完全被置换出,滤渣A中含有过量的铁粉、铜、汞,然后加入适量的稀硫酸把过量的铁粉除去,铁与稀硫酸反应生成硫酸亚铁和氢气,铜、汞不与稀硫酸反应,在滤渣中;判断加入稀硫酸“适量”的实验现象是:溶液中恰好没有气泡产生;故填:使废液的Hg(NO3)2、Cu(NO3)2中 Hg、Cu完全被置换出;Fe+H2SO4=FeSO4+H2↑;溶液中恰好没有气泡产生;
(3)滤渣D包括Hg、Cu,给滤渣加热时,Cu就变成了黑色固体氧化铜CuO,其转化为Cu的反应是氧化铜和一氧化碳在加热的条件下生成铜和二氧化碳,化学方程式是: CuO+CO![]() Cu+CO2;CuO失去氧,发生了还原反应。故填:CuO+CO
Cu+CO2;CuO失去氧,发生了还原反应。故填:CuO+CO![]() Cu+CO2;CuO
Cu+CO2;CuO
(4)为防止有毒的汞蒸气扩散污染环境,冷凝回收汞的操作应盛有水的仪器中或有冷凝功能的密闭装置中,故答案为:①④

 学期复习一本通学习总动员期末加暑假延边人民出版社系列答案
学期复习一本通学习总动员期末加暑假延边人民出版社系列答案 芒果教辅暑假天地重庆出版社系列答案
芒果教辅暑假天地重庆出版社系列答案