题目内容
【题目】根据如图回答有关的实验问题。
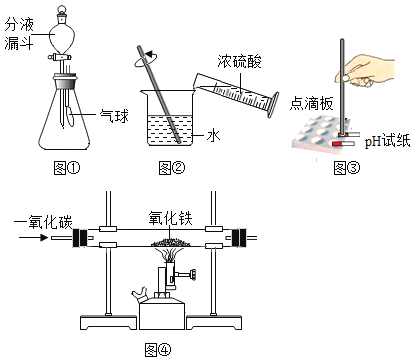
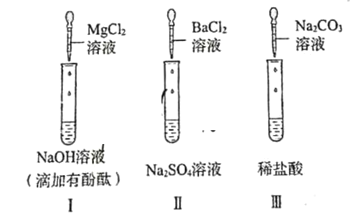
(1)图①锥形瓶中充满二氧化碳,将分液漏斗中的氢氧化钠溶液加入到瓶中,观察到的现象是__________,原理是_____________________(用化学方程式表示);
(2)图②操作中用玻璃棒搅拌的目的是______;
(3)图③探究硫酸铜溶液的酸碱性,用pH试纸测得pH<7,说明硫酸铜溶液呈_____性;
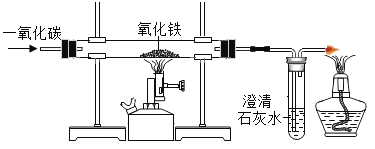
(4)图④实验中玻璃管中的现象是___________________,反应的化学方程式为______________________。
【答案】气球膨胀(变大) CO2+2NaOH=Na2CO3+H2O 散热,防止液体飞溅 酸 红棕色固体变慢逐渐变为黑色 Fe2O3+3CO![]() 2Fe+3CO2
2Fe+3CO2
【解析】
(1)图①锥形瓶中充满二氧化碳,将分液漏斗中的氢氧化钠溶液加人到瓶中,二氧化碳能与氢氧化钠反应产生碳酸钠和水的化学方程式:CO2+2NaOH=Na2CO3+H2O,装置内压强变小,观察到的现象是:大气压使气球膨胀(变大);
(2)图②稀释浓硫酸操作中用玻璃棒搅拌的目的是:使溶液散热,防止液体飞溅;
(3)图③探究硫酸铜溶液的酸碱性,用pH试纸测得pH<7,说明硫酸铜溶液呈酸性;
(4)图④实验中一氧化碳在高温条件下与氧化铁反产生铁和二氧化碳,玻璃管中的现象是:红棕色固体变慢逐渐变为黑色;反应的化学方程式:Fe2O3+3CO![]() 2Fe+3CO2。
2Fe+3CO2。

【题目】为了测定液化气中丙烷(C3H8)在氧气不足时的燃烧产物,将一定量的丙烷和氧气置于一个封闭的容器中引燃,测得反应前后各物质的质量如下表:
物质 | 丙烷 | 氧气 | 水 | 二氧化碳 | X |
反应前质量/g | 4.4 | 12.8 | 0 | 0 | 0 |
反应后质量/g | 0 | 0 | 7.2 | 4.4 | a |
下列判断正确的是
A.表中a的值为5.6 B.X可能是该反应的催化剂
C.X可能含有氢元素 D.X只含碳元素