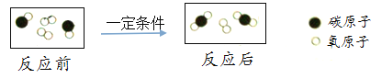
题目内容
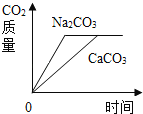
【题目】将等质量的CaCO3(块状)和Na2CO3(粉末),分别浸入一定量10%盐酸和10%硫酸溶液中,产生CO2的质量随时间变化曲线如图所示,下列说法正确的是( )
A.CaCO3一定没有剩余 B.消耗HCl与H2SO4的质量比为73:98
C.消耗CaCO3与Na2CO3的质量比为1:1 D.反应产生水的质量相等
【答案】BD
【解析】
试题分析:CaCO3(块状)和Na2CO3(粉末)与盐酸和硫酸分别反应的方程式是:CaCO3+2HCl═CaCl2+H2O+CO2↑,
100 73 18 44
Na2CO3+H2SO4═Na2SO4+H2O+CO2↑;
106 98 18 44
观察图象可知:二者生成的二氧化碳的质量相等,据方程式和物质之间的质量关系可知:生成的水的质量也相等,则D正确,参加反应的盐酸和硫酸的质量比是73:98,B正确;
参加反应的碳酸钙和碳酸钠的质量比是100:106,故C错误,提供的碳酸钙和碳酸钠的质量相等,说明碳酸钠完全反应,碳酸钙有剩余,则A错误;故选:BD.

练习册系列答案
 初中学业考试导与练系列答案
初中学业考试导与练系列答案
相关题目
【题目】某兴趣小组的同学为了测定碳酸钠样品(只含有氯化钠,不含其它杂质)中碳酸钠的含量,取该混合物样品与适量稀盐酸恰好完全反应,有关实验数据见附表.
附表:实验数据
反应前 | 反应后 | |||
实验数据 | 烧杯的质量/g | 稀盐酸的质量/g | 混合物样品的质量/g | 烧杯和其中混合物的质量/g |
40.6 | 123.4 | 12 | 171.6 | |
(1)反应生成二氧化碳的质量为 g;
(2)样品碳酸钠的质量分数是多少?(最后结果保留到0.1%)
(3)反应后所得溶液的溶质质量分数是多少?