题目内容
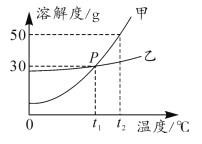
【题目】如图是甲、乙两种固体(不含结晶水)的溶解度曲线。t1°C时,若乙溶液中溶剂与溶质的质量比为5 : 1,则该溶液属于_____________(填“饱和”或“不饱和”)溶液;t2°C时,等质量甲、乙的饱和溶液中溶剂的质量:甲_______________乙(填“>”“<”或“=”);若甲中混有少量乙,则提纯甲的方法是_____________。
【答案】不饱和 < 降温结晶(或冷却热饱和溶液)
【解析】
t1°C时,乙的溶解度是30g,即乙的饱和溶液中溶剂和溶质的质量比为100:30=10:3,若乙溶液中溶剂与溶质的质量比为5:1,则该溶液属于不饱和溶液;
t2°C时,甲的溶解度大于乙,等质量甲、乙的饱和溶液中溶质的质量:甲>乙,则溶剂的质量:甲<乙;
甲的溶解度随温度升高而增大,且随温度变化较大,若甲中混有少量乙,则提纯甲的方法是降温结晶(或冷却热饱和溶液)。

【题目】对比实验是实验探究的重要方法,下列对比实验设计能实现相应实验目的的是( )
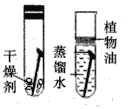
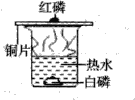
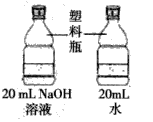
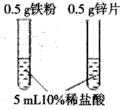
A探究空气对铁生锈的影响 | B探究燃烧需要温度达到着火点 | C探究 | D比较锌和铁的金属活动性 |
|
|
|
|
A.AB.BC.CD.D
【题目】在密闭容器有甲、乙、丙、丁四种物质,在一定条件下让其充分反应,测得反应前后各物质的质量变化如下表所示:
物 质 | 甲 | 乙 | 丙 | 丁 |
反应前的质量/g | 50 | 23 | 1 | 3 |
反应后的质量/g | 2 | x | 45 | 30 |
下列说法中,正确的是
A.甲一定是化合物B.x的值等于0
C.丙和丁的质量变化比为3:2D.该反应是分解反应
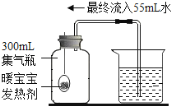
【题目】化学实验活动课上,同学们利用了如图所示实验探究氢氧化钙的性质。
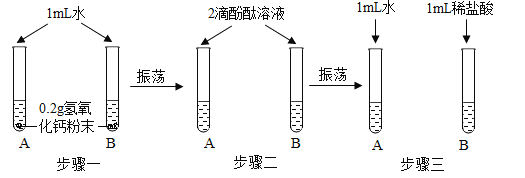
(1)上述三个步骤的A试管中固体始终无明显减少,那么能说明A试管的水中溶有氢氧化钙的现象是__________。
(2)步骤三试管B中溶液变无色,发生反应的化学方程式_______________。
小明的实验:小明直接把稀盐酸滴入盛有氢氧化钙溶液的试管中,始终没有看到明显变化。
(提出问题)小明实验后试管中溶质的成分是什么?
(查阅资料)CaCl2溶液显中性。
(猜想与假设)针对疑问,甲组同学猜想如下:
猜想I:只有CaCl2猜想Ⅱ有________
猜想Ⅲ:有CaCl2和Ca(OH)2
猜想Ⅳ:有CaCl2、HCl和Ca(OH)2
乙组同学对以上猜想提出质疑,认为猜想Ⅳ不合理,其理由是_____________
(实验探究)为了验证其余猜想,各小组进行了下列三个方案的探究。
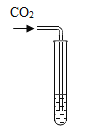
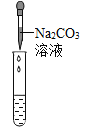
实验方案 | 滴加紫色石蕊试液 | 通入CO2 | 滴加Na2CO3 |
实验操作 |
|
|
|
实验现象 | _________ | __________ | 产生白色沉淀 |
实验结论 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 | 溶液中含有Ca(OH)2 |
(得出结论)通过探究,全班同学一致确定猜想Ⅲ是正确的。
(评价反思)丙组同学认为滴加Na2CO3溶液产生白色沉淀,并不能证明溶液中一定含有Ca(OH)2,请你帮助他们说明原因_____________。