题目内容
【题目】乙二酸俗称草酸,各种植物都含有草酸,其中以菠菜、茶叶中含量最多。某兴趣小组的同学对草酸晶体的组成进行了下列探究。
(查阅资料)
(1)草酸是一种有机酸。
(2)草酸在加热条件下分解能生成三种化合物。
(实验探究)
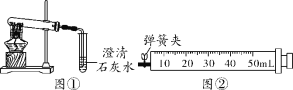
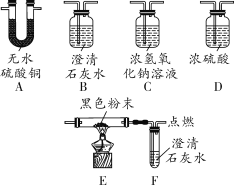
(1)兴趣小组同学取草酸隔绝空气加热,将分解产生的气体先通入A装置,发现无水硫酸铜变蓝,再通入B装置,发现澄清石灰水变浑浊,由此证明草酸分解有____和水生成,从而推断出草酸中含有___元素。
(2)小明认为A、B装置颠倒顺序不会影响验证结果,你是否同意他的观点,请说明原因_______。
(3)小红根据草酸的组成元素及查阅资料的内容,猜想草酸分解也可能有一氧化碳生成,于是继续探究。小红将B装置中导出的气体通入C、D装置,其中C装置中发生反应的化学方程式为________,再依次通过E、F装置,发现E装置中黑色粉末变红,F装置中澄清石灰水变浑浊,由此证明了她的猜想,则E装置中黑色粉末的化学式为_____。
(实验结论)最终同学们得出了草酸的组成元素。
(拓展延伸)
(1)装置F处点燃尾气的原因是_______。
(2)研究物质组成的常用方法是:根据化学反应前后____不变的原则,考虑被探究物质的化学性质,设计实验让物质参与一个化学反应,通过分析反应物或生成物的元素组成进一步确定该物质的组成元素。
【答案】二氧化碳 碳、氢、氧 不同意,若A、B颠倒则无法证明生成的气体中是否含有水蒸气 CO2+2NaOH=Na2CO3+H2O CuO 防止尾气对空气造成污染 元素种类
【解析】
【实验探究】(1)实验中草酸隔绝空气加热将分解的产物通入无水硫酸铜,无水硫酸铜变蓝,说明生成的气体中含有水蒸气;二氧化碳能使澄清石灰水变浑浊,所以B中澄清石灰水变浑浊,说明草酸分解有二氧化碳生成,根据反应前后元素种类不变,可推知草酸中含有碳、氢、氧三种元素。(2)若A、B颠倒,则也可能是从澄清石灰水中带出的水蒸气使无水硫酸铜变蓝,从而无法证明生成的气体中是否含有水蒸气。(3)因原气体中有二氧化碳,会影响一氧化碳的验证,所以要先除去二氧化碳并将气体干燥,C中浓氢氧化钠溶液的作用是除去二氧化碳,反应的化学方程式为CO2+2NaOH=== Na2CO3+H2O,一氧化碳与氧化铜反应可生成红色的铜单质和二氧化碳,所以E处黑色粉末为氧化铜。【拓展延伸】(1)由于尾气中可能含有CO,因此尾气经点燃处理能防止对空气造成污染。(2)根据质量守恒定律,反应前后元素种类不变,再通过实验分析反应物或生成物的元素组成进一步确定该物质的组成元素。

 中考解读考点精练系列答案
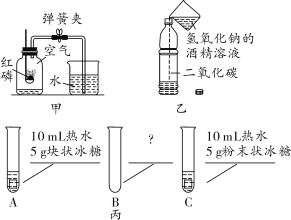
中考解读考点精练系列答案【题目】(2018石家庄长安区质检)某研究小组发现,维C泡腾片(保健药品,主要成分见图1)溶于水,有许多气泡产生(如图2),该小组同学进行如下研究。

探究一:该气体的成分
(猜想与假设)小王说:该气体可能是CO2、O2、CO、H2、N2。
小李说:不可能含有CO和H2,因为从药品安全角度考虑,CO有毒,H2________________。
小张说:不可能含有N2,因为___________。
该小组同学认为:该气体可能含有CO2、O2中的一种或两种。
(进行实验)
实验编号 | 实验操作 | 实验现象 |
① | 将气体通入澄清石灰水中 | 澄清石灰水变浑浊 |
② | 将带火星的木条伸入该气体中 | 带火星的木条没有复燃 |
(得出结论)
(1)由实验①可知,该气体中肯定含有________,写出该反应的化学方程式________。
(2)由实验②不能确定该气体中不含氧气,理由是_____________。
若要证明含有氧气,请你帮助设计实验_____________。
探究二:维C泡腾片溶液的酸碱性
(3)向维C泡腾片溶液中滴加石蕊溶液,溶液变红,说明溶液显________性。
【题目】化学实验过程经常会产生一定量的废液,经过无害化处理可有效防止水体污染。在一次实验课上,兴趣小组的同学们完成了NaOH溶液和Na2CO3溶液的鉴别,并对废液成分展开探究。
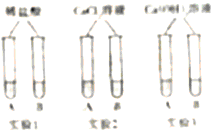
活动一
通过小组合作,同学们完成了右图所示的三组小实验。实验中生成白色沉淀的化学方程式是____________________(写一个)。
活动二
小雪将六支试管中的剩余物倒入一个洁净的大烧杯中(如下图), 充分搅拌、静置。观察到杯内上层是无色溶液,下层有白色沉淀。由此可以确定:上层溶液中一定不含有的离子是__________________、以及一定含有的离子。小组同学对上层溶液中还可能含有的离子进行了如下探究。![]()
(提出问题)上层溶液中还可能含有什么离子?
(猜想与假设)上层溶液中还可能含有OH-、CO32-、Ca2+中的一种或几种。
(进行实验)
实验步骤 | 实验现象 | 实验结论 | |
方案一 | ①取少量溶液于试管中,滴加无色酚酞溶液②继续滴加稀盐酸 | ①溶液变红 ②产生气泡 | ①有OH- ②有CO32-、无Ca2+ |
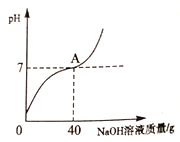
方案二 | 取少量溶液于试管中,____________(指示剂除外) | ①____________ ②___________ | ①有CO32-、无Ca2+ ②有OH- |
(反思与评价)
(1)小明同学对方案一提出质疑, 他的理由是________________________。
(2)经过综合分析,最终确定上层溶液中肯定存在的离子有______________________。
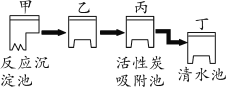
(3)将烧杯内物质过滤,滤渣回收,向滤液中加入适量_______________________进行处理后再排放。
【题目】我国发行的第五套人民币中,铸造1元、5角和1角硬币的主要材料含有铁、镍(Ni)、铜等。

(查阅资料)氯化镍溶液为绿色。
(猜想假设)根据所学知识,猜想三种金属在金属活动性顺序中的相对位置关系:
猜想一:Fe>Cu>Ni 猜想二:Ni>Fe>Cu猜想三: ____
(实验探究)兴趣小组的同学设计了以下两种方案来进行探究,都得出了相同的实验结论。
实验方案 | 实验步骤 | 实验现象 | 实验结论 |
方案一 | (1)把一根光亮的铁丝放入盛有NiCl2溶液的试管中 | 铁丝表面有固体析出 | |
(2)把一根镍丝插入盛有CuCl2溶液的试管中 | 镍丝表面有___析出 | ||
方案二 | 分别取三支试管,向其中加入等质量、等浓度的稀盐酸,然后将铁、镍、铜三种金属丝分别插入三支试管中 | ____,加入铁丝、镍丝的试管中溶液变为浅绿色 | 猜想__成立。铁丝与稀盐酸反应的化学方程式为_____ |
(分析讨论)将铁丝打磨光亮的目的是______。
(反思交流)在NiCl2和CuCl2的混合溶液中加入一定量的铁粉,充分反应后过滤得到滤渣,向滤渣中加入足量稀盐酸,有气泡产生,则滤渣中一定含有的物质是__(填化学式)。