题目内容
【题目】化学实验过程经常会产生一定量的废液,经过无害化处理可有效防止水体污染。在一次实验课上,兴趣小组的同学们完成了NaOH溶液和Na2CO3溶液的鉴别,并对废液成分展开探究。
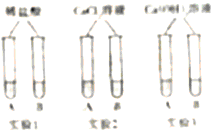
活动一
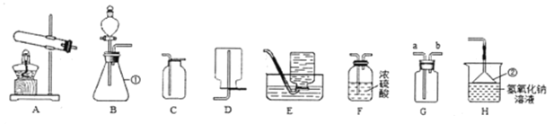
通过小组合作,同学们完成了右图所示的三组小实验。实验中生成白色沉淀的化学方程式是____________________(写一个)。
活动二
小雪将六支试管中的剩余物倒入一个洁净的大烧杯中(如下图), 充分搅拌、静置。观察到杯内上层是无色溶液,下层有白色沉淀。由此可以确定:上层溶液中一定不含有的离子是__________________、以及一定含有的离子。小组同学对上层溶液中还可能含有的离子进行了如下探究。![]()
(提出问题)上层溶液中还可能含有什么离子?
(猜想与假设)上层溶液中还可能含有OH-、CO32-、Ca2+中的一种或几种。
(进行实验)
实验步骤 | 实验现象 | 实验结论 | |
方案一 | ①取少量溶液于试管中,滴加无色酚酞溶液②继续滴加稀盐酸 | ①溶液变红 ②产生气泡 | ①有OH- ②有CO32-、无Ca2+ |
方案二 | 取少量溶液于试管中,____________(指示剂除外) | ①____________ ②___________ | ①有CO32-、无Ca2+ ②有OH- |
(反思与评价)
(1)小明同学对方案一提出质疑, 他的理由是________________________。
(2)经过综合分析,最终确定上层溶液中肯定存在的离子有______________________。
(3)将烧杯内物质过滤,滤渣回收,向滤液中加入适量_______________________进行处理后再排放。
【答案】 Ca(OH)2+Na2CO3 =CaCO3↓+2NaOH(或CaCl2+Na2CO3=CaCO3↓+2NaCl) H+(或氢离子) 滴加过量的BaCl2溶液,静置,继续滴加CuSO4溶液,(或滴加过量的Ca(NO3)2溶液,静置,继续滴加FeCl3溶液。 产生白色沉淀 产生蓝色沉淀(或产生红褐色沉淀) 溶液中有CO32-(或Na2CO3)也会使酚酞变红,无法判断是否含OH-[或溶液中有CO32-(或Na2CO3)溶液也显碱性,无法判断是否含OH-](合理即可) Na+、 Cl-、OH-、CO32- (或钠离子、氯离子、氢氧根离子、碳酸根离子) 稀硫酸(或稀盐酸/酸)
【解析】活动一、根据氢氧化钙溶液与碳酸钠溶液反应生成碳酸钙和氢氧化钠(或氯化钙溶液与碳酸钠溶液反应生成碳酸钙和氯化钠)解答;活动二、根据烧杯下层的白色沉淀应为碳酸钙,说明盐酸反应完,据此分析解答;【进行实验】根据检验碳酸根可以加入钙离子的溶液或钡离子的溶液;检验氢氧根离子可以加入能够说出碱性沉淀的离子分析解答;【反思与评价】(1)根据碳酸钠溶液显碱性,也能使无色酚酞溶液变红解答;(2)根据实验分析解答;(3)根据酸碱中和解答。活动一、氢氧化钙溶液与碳酸钠溶液反应生成碳酸钙和氢氧化钠,反应的化学方程式为Ca(OH)2+Na2CO3 =CaCO3↓+2NaOH(或氯化钙溶液与碳酸钠溶液反应生成碳酸钙和氯化钠,反应的化学方程式为CaCl+Na2CO3=CaCO3↓+2NaCl);活动二、烧杯下层的白色沉淀应为碳酸钙,说明盐酸反应完,故上层溶液中一定不含有的离子是H+(或氢离子);【进行实验】实验步骤:滴加过量的BaCl2溶液,静置,继续滴加CuSO4溶液(或滴加过量的Ca(NO3)2溶液,静置,继续滴加FeCl3溶液]; 现象:①产生白色沉淀;②产生蓝色沉淀(或产生红褐色沉淀);【反思与评价】(1)溶液中有CO32-(或Na2CO3)也会使酚酞变红,无法判断是否含OH-[或溶液中有CO32-(或Na2CO3)溶液也显碱性,无法判断是否含OH-] ;(2)碳酸钠与盐酸反应生成氯化钠和水;碳酸钠与氯化钙反应生成碳酸钙和氯化钠;碳酸钠与氢氧化钙溶液反应生成碳酸钙和氢氧化钠,故经过综合分析,最终确定上层溶液中肯定存在的离子有 Na+、 Cl-、OH-、CO32- (或钠离子、氯离子、氢氧根离子、碳酸根离子);(3)滤液中含有氢氧化钠、碳酸钠等碱性物质,应加稀硫酸(或稀盐酸或酸)进行处理后再排放。