��Ŀ����
����Ŀ��һƿ���ڷ��õ��������ƹ��壬ͬѧ����̽�����Ƿ���ʣ�����һͬ���벢�ش��й����⡣
(1)д�����������ڿ����б��ʵĻ�ѧ��Ӧ����ʽ___________________________��
��������룩
����1����ƿ����ijɷ���NaOH��
����2����ƿ����ijɷ���_________��
����3����ƿ����ijɷ���NaOH��Na2CO3�Ļ���
���������ϣ���Na2CO3+HCl=NaCl +NaHCO3��NaHCO3+HCl=NaCl +CO2��+H2O����BaCl2��Һ�����ԣ����������ι�ͬ��Ӧʱ������кͷ�Ӧ���Ƚ��С�
��ʵ����̽�֣�
ȡ������Ʒ���ձ��У�������������ˮ������Ʒȫ���ܽ⡣
(2)ȡ������Һ���Թ��У������м�����ɫ��̪��Һ����Һ����ɫ��Ϊ��ɫ����ͬѧ��Ϊ����1��ȷ����ͬѧ��Ϊ��ͬѧ�Ľ��۲���ȷ����������_____________________��
(3)��(2)��Һ�м��������BaCl2��Һ������________________���������3��ȷ��������Ӧ�Ļ�ѧ����ʽΪ_________________��
(4)��ͬѧ��ȡ������Һ���Թ��У���������ϡ���ᣬû�п������ݲ�����������ų��˲���2�Ͳ���3��������2�����3��ȷ������ϡ���ᷢ����Ӧ�Ļ�ѧ����ʽ�ֱ�Ϊ_________��___________��
���������ۣ�
(5)��ͬѧ��ΪBaCl2��ҺҲ������Ba(OH)2��Һ�������ʵ�飬ͬѧ��һ����Ϊ��ͬѧ�������Ǵ���ģ�������������___________________________________________��
(6)ͨ���������Ʊ��ʵ��о���֪�������տ����е�H2O��O2��CO2�������ܹ����ʵ�ҩƷ�����ܷⱣ�棬���о���һ����Ҫ�ܷⱣ���ҩƷ�����ӣ���_______________________��
(7)ȡ9.3g���ֱ��ʵ�NaOH��Ʒ������������ˮ�����Һ������Һ�в��ϼ���7.3%��ϡ���ᣬʵ���м���ϡ���������������������ϵ��ͼ��ʾ��
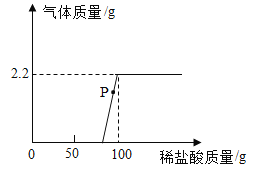
��P����Һ�����ʵijɷ���_______________(д��ѧʽ)��
�ڸ���Ʒ�ı�����Ϊ_________(���ʵ�NaOH��ԭNaOH�������ٷֱ�)��
���𰸡�CO2+2NaOH=Na2CO3+H2O Na2CO3 Na2CO3��Һ�Լ��ԣ�Ҳ��ʹ��̪��Һ��� ��ɫ�������ɣ���Һ�Գʺ�ɫ BaCl2+Na2CO3=BaCO3��+2NaCl Na2CO3+HCl=NaCl+NaHCO3 NaOH+HCl=NaCl+H2O(����ʽ˳��ߵ����) ����Ba(OH)2������OH-�������˶�ԭ��Һ��NaOH�ļ��� ������ NaCl ��NaHCO3 50%
��������
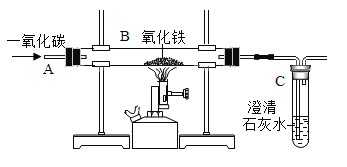
��1�����������ڿ����б��ʣ�����Ϊ�������ƺͶ�����̼��Ӧ����̼���ƺ�ˮ����Ӧ�Ļ�ѧ��Ӧ����ʽ��2NaOH+CO2�TNa2CO3+H2O��
[�������]
����1��û�б���ʱ��ƿ����ijɷ���NaOH��
����2��ȫ������ʱ��ƿ����ijɷ���̼���ƣ�
����3�����ֱ���ʱ��ƿ����ijɷ���NaOH��Na2CO3�Ļ���
��2����ͬѧ��Ϊ��ͬѧ�Ľ��۲���ȷ����������̼������Һ�Լ��ԣ�Ҳ��ʹ��̪��Һ���ɫ��
��3����2����Һ�м��������BaCl2��Һ����������ɫ�������Ȼ�����̼���Ʒ�Ӧ���ɰ�ɫ����̼�ᱵ������Һ��Ȼ�Ǻ�ɫ����Һ�к����������ƣ��������3��ȷ��������Ӧ�Ļ�ѧ����ʽΪ��BaCl2+Na2CO3�TBaCO3��+2NaCl��
��4��������2��������̼���ƺ����ᷴӦ����̼�����ƺ��Ȼ��ƣ�̼�����ƺ����ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼��������3��ȷ����������������Ʒ�Ӧ�����Ȼ��ƺ�ˮ��̼���ƺ����ᷴӦ����̼�����ƺ��Ȼ��ƣ�̼�����ƺ����ᷴӦ�����Ȼ��ơ�ˮ�Ͷ�����̼������ϡ���ᷢ����Ӧ�Ļ�ѧ����ʽ�ֱ�ΪNa2CO3+HCl�TNaCl+NaHCO3��NaHCO3+HCl�TNaCl+CO2��+H2O��NaOH+HCl�TNaCl+H2O��Na2CO3+HCl�TNaCl+NaHCO3��NaHCO3+HCl�TNaCl+CO2��+H2O��
��5����ͬѧ��ΪBaCl2��ҺҲ������Ba��OH��2��Һ�������ʵ�飬ͬѧ��һ����Ϊ��ͬѧ�������Ǵ���ģ�����������������������̼���Ʒ�Ӧ�����������ƣ�Ӱ����������Ƶļ��顣
��6���������ܺ�ˮ��Ӧ�����������ƣ������Ҫ�ܷⱣ�档
��7���⣺��P����Һ�����ʵijɷ��Ƿ�Ӧ���ɵ��Ȼ��ƺͲ���û�з�Ӧ��̼�����ơ�
����̼��������Ϊ![]() ��
��
��Na2CO3+HCl�TNaCl+NaHCO3��NaHCO3+HCl�TNaCl+CO2��+H2O��֪��Na2CO3+2HCl�T2NaCl+H2O+CO2����
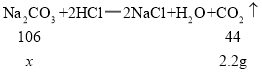
![]()
![]() =5.3g��
=5.3g��
��Ʒ����������������9.3g-5.3g=4g��
����ʵ�������������Ϊ![]() ��
��
2NaOH+CO2�TNa2CO3+H2O��
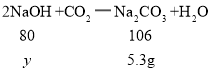
![]()
![]() =4g��
=4g��
��Ʒ�ı�����Ϊ��![]() ��100%=50%��
��100%=50%��
�𣺸���Ʒ�ı�����Ϊ50%��

 �Ķ��쳵ϵ�д�
�Ķ��쳵ϵ�д�