题目内容
【题目】2019年我国首艘国产航母山东舰正式入列,中国海军正式迈入双航母时代。
(1)建造航母用到了钛合金,构成金属钛的粒子是____( 填“原子”“分子”或“离子”),工业制钛有一种反应为:![]() , X的化学式为________。
, X的化学式为________。
(2)航母外壳用涂料覆盖,是为了防止钢铁材料与________接触而锈蚀,而金属铝在空气中更耐腐蚀的原因是_________(用化学方程式表示) .
(3)为了探究航母材料中锌、铁、铜三种金属活动性强弱,某同学设计了下列实验(每步均充分反应),其中能达到目的是_________(填序号)。
A 稀盐酸中加入足量铁粉后,再加铜粉,最后加入锌粉
B ZnCl2 溶液中加入足量铁粉后,再加入CuCl2溶液
C ZnCl2 溶液中加入足量铜粉后,再加入铁粉
(4)向含有氯化铜、氯化锌、稀盐酸的混合溶液中加入过量铁粉,充分反应后过滤,滤液中含有的溶质是_______(写化学式)。
(5)有一包金属粉末,可能由Mg、Zn、Fe、Al、Ag等金属中的一种或几种组成。取该样品4.8 g加入100g稀硫酸恰好完全反应,只得到0.4g H2和无色溶液,下列说法正确的是______
A 样品中一定只含有Mg
B 样品中一定不含有Ag,可能含有Fe
C 稀硫酸的溶质质量分数为9.8%
D 无色溶液中溶质总质量为24 g
【答案】原子 SO3 水、氧气 ![]() AB ZnCl2、FeCl2 D
AB ZnCl2、FeCl2 D
【解析】
(1)金属是由原子直接构成的,构成金属钛的粒子是原子;工业制钛有一种反应为:![]() ,由质量守恒定律反应前后原子的种类及数目不变可知,反应物中有1个钛原子,4个氟原子,4个氢原子,2个硫原子,8个氧原子,生成物中含有4个氢原子,4个氟原子,1个钛原子,2个氧原子,故2个X中有2个硫原子和6个氧原子,所以X的化学式为:SO3;
,由质量守恒定律反应前后原子的种类及数目不变可知,反应物中有1个钛原子,4个氟原子,4个氢原子,2个硫原子,8个氧原子,生成物中含有4个氢原子,4个氟原子,1个钛原子,2个氧原子,故2个X中有2个硫原子和6个氧原子,所以X的化学式为:SO3;
(2)铁在潮湿的空气中易生锈,航母外壳用涂料覆盖,是为了防止钢铁材料与水、氧气接触而锈蚀,而金属铝在空气中更耐腐蚀的原因是铝与氧气反应生成致密的氧化铝薄膜,反应的方程式为![]() ;
;
(3)A、稀盐酸中加入足量铁粉后,生成了氯化亚铁和氢气,再加铜粉,不反应,说明了铁的金属活动性大于铜,最后加入锌粉,能将铁置换出来,说明了锌的活动性大于铁,可以比较金三种属的活动性强弱,故A正确;
B、ZnCl2溶液中加入足量铁粉后,不反应,说明了锌的活动性大于铁,再加入CuCl2溶液,铁与氯化铜反应,说明了铁的活动性大于铜,可以比较三种金属的活动性强弱,故B正确;
C、ZnCl2溶液中加入足量铜粉,不反应,说明锌的活动性比铜强,再加入铁粉,也不反应,说明了锌的活动性大于铁,但不能比较铜和铁的活动性强弱,不可以比较三种金属的活动性强弱,故C错误。
故选AB。
(4)由金属活动性顺序表可知,锌>铁>氢>铜。在ZnCl2、CuCl2和盐酸混合溶液中加入过量的铁粉时,铁与盐酸反应生成氯化亚铁和氢气;铁能与氯化铜反应生成氯化亚铁和铜,不能与氯化锌反应。充分反应后,过滤,滤液中无氯化铜,有生成的氯化亚铁和原来的氯化锌,故填:ZnCl2、FeCl2。
(5)A、铁与盐酸反应生成浅绿色氯化亚铁溶液,银不与稀盐酸反应,反应后只得到氢气和无色溶液,说明样品中没有铁或银,设与足量的盐酸反应生成0.4g氢气消耗镁、锌和铝的质量分别为x、y、z,



![]()
![]()
![]()
解得x=4.8g ,y=13g,z=3.6g
故该样品可能只含有镁,也可能锌和铝或镁、锌和铝的混合物,故A错误;
B、Mg、Zn、Fe、Al均与稀硫酸发生置换反应,生成的氯化亚铁是浅绿色的,氯化镁、氯化锌和氯化铝溶液均为无色的,Ag不与稀硫酸发生反应。样品与稀硫酸恰好完全反应,且只得到氢气和无色溶液,可知,样品中一定没有铁,也没有不与稀硫酸反应的银,故B错误;
C、根据氢元素质量守恒,稀硫酸中溶质质量为:![]() ,稀硫酸的溶质质量分数为
,稀硫酸的溶质质量分数为![]() ,故C错误;
,故C错误;
D、无色溶液中溶质总质量为100g+4.8g-0.4g-(100g-19.6g)=24g,故D正确。
故选D。

【题目】2020年1月25日总建筑面积为3.39万平方米的火神山医院正式开工,火神山医院在建造过程中用到了HDPE膜. HDPE膜具有极好的抗冲击性和防潮性,某探究小组对HDPE膜的组成元素进行了如下探究。
[提出问题] HDPE膜由什么元素组成?
[查阅资料]①HDPE膜能够燃烧,燃烧可能生成一氧化碳;
②碱石灰主要成分是氢氧化钠固体和氧化钙固体。
[实验探究]如图所示,先通入干燥氮气,再将4.2g的HDPE膜样品在一定质量的氧气中点燃,并将燃烧产物依次通过装置A、B、C、D (装置中每步反应均进行完全)。
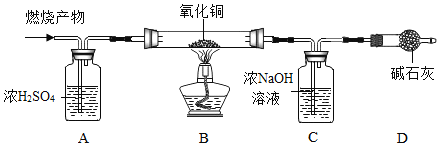
[实验记录]
装置质量 | A装置总质量 | C装置总质量 |
实验前 | 100.0g | 100.0g |
实验后 | 105.4g | 113.2g |
[实验分析]
(1)装置A中浓硫酸的作用是________。
(2)实验中观察到装置B中黑色粉末变成红色,证明燃烧产物中有________。
(3)装置B中发生的化学反应方程式为_________。
(4)分析反应后装置C中的溶质。取适量C中溶液于烧杯中,加入______溶液, 静置,再滴加____;产生白色沉淀,溶液变红色;则溶液中含有的溶质是_____。
[实验结论]
(5)HDPE膜由元素_____(填元素符号)组成。
(6)某工厂每天要烧掉含硫1.6%的烟煤100吨,排放出的SO2严重地污染环境。如果用石灰乳吸收这些二氧化硫,至少需要熟石灰________吨。