题目内容
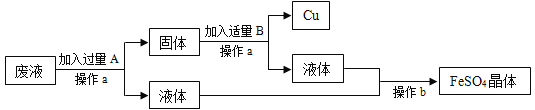
【题目】(2016唐山路南区二模)从X、银、铜、锌四种金属混合物中分离某贵重金属的流程如图:
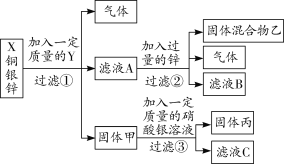
下列有关叙述中不正确的是( )
A.Y可能是稀硫酸
B.固体丙中一定含有银
C.根据上述流程无法完全比较出四种金属的活动性强弱
D.四种金属的活动性顺序由强到弱依次是:锌、X、铜、银
【答案】C
【解析】
金属与酸反应才有气体生成,当向四种金属混合物中加入Y时,生成气体,说明Y是一种酸,可能是稀硫酸,A正确;向滤液A中加入过量的锌,仍有气体生成,说明加入的Y即稀硫酸过量。固体甲中一定含有铜和银,铜和硝酸银反应产生硝酸铜和银,因此固体丙中一定含有银,B正确;根据金属的活泼性顺序:锌>氢>铜>银,故向锌、X、铜、银的金属混合物中加入稀硫酸,锌一定参加反应并产生气泡,而铜和银一定没反应,得到的滤液A再加入过量的锌得到固体混合物乙和滤液B,说明锌除了和过量的稀硫酸反应产生气体外,还和盐溶液发生了置换反应,而铜和银没有参加反应,因此是锌和X的盐溶液发生的反应,因此说明锌的活动性比X强,且X位于氢前,D正确、C错误。故选C。

练习册系列答案
相关题目
【题目】下列应用的叙述、对应的化学方程式及基本反应类型均正确的是( )
选项 | 用途 | 化学原理(用化学方程式表示) | 基本反应类型 |
A | 高炉炼铁 | 3CO+2Fe2O3═2Fe+3CO2 | 置换反应 |
B | 稀盐酸用于除铁锈 | Fe2O3+2HCl═FeCl2+2H2O | 化合反应 |
C | 用熟石灰处理硫酸厂废液 | Ca(OH)2+H2SO4═CaSO4+2H2O | 复分解反应 |
D | 电解水制氢气 | 2H2O═2H2+O2 | 分解反应 |
A. A B. B C. C D. D