题目内容
【题目】氢气的储存是科学研究热点之一。X是一种储存氢气的材料,取11.2g X在O2中完全燃烧后只生成8.0g CuO、8.0g MgO。
(1)上述燃烧过程中消耗O2的质量为多少克。
(2)通过计算求X中各元素的原子个数比。(写出计算过程)
【答案】(1)4.8(2)1:2(详见解析)
【解析】
根据质量守恒定律,由生成物可以初步确定该物质中含有铜元素和镁元素,由生成的氧化铜和氧化镁中铜、镁元素的质量和与该物质的质量进行对比,从而确定X中各元素的原子个数比。
(1)根据参加反应的物质等于生成物的质量,可知消耗氧气的质量为![]() ;
;
(2)8.0g CuO中含有铜元素的质量![]()
8.0g MgO中含有镁元素的质量![]()
因为m铜+m镁=6.4g+4.8g=11.2g;
所以X中只含有铜、镁元素,故可设该物质的化学式为CuxMgy;
因为m铜:m镁=64x:24y=6.4g:4.8g
所以x:y=1:2。
则X中铜、镁元素的原子个数比为1:2。

 考前必练系列答案
考前必练系列答案【题目】我国是世界化肥第一生产大国和消费大国。以空气和煤炭等为化工原料,可合成氨、尿素(CO(NH2)2),主要生产工艺流程如下图所示。回答下列问题:
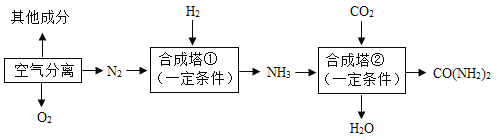
(1)工业合成氨的原料是氮气和氢气,氮气可从空气分离中获得。从液态空气中分离出N2的过程属于____(填“物理”或“化学”)变化。空气中含量少量的稀有气体,其化学性质极为_____(填“活泼”或“稳定”)。
(2)氢气通过煤和水蒸气在高温时反应得到的合成气(H2、CO)提取,制备合成气前需先将煤粉碎,这样做的目的是_____,反应的基本类型为________。
(3)写出合成塔①中合成氨的化学方程式为________。尿素属于_____(填“氮”“钾”“磷”或“复合”)肥。
(4)压强为101kPa下,氨气在不同温度下的溶解度如下表。氨水是氨气的水溶液,贮存时氨水要注意_____。
温度/℃ | 10 | 20 | 30 | 60 |
溶解度/g | 70 | 56 | 44.5 | 20 |
(5)2019年全国节能宣传周主题为“绿色发展,节能先行”。其中符合要求的___(填序号)
A 烟囱中排放出未经处理的烟尘、废水和废气
B 综合采用煤的洁净化技术
C 循环利用氮气、氢气和水
【题目】某化学小组探究炼铁的反应原理。
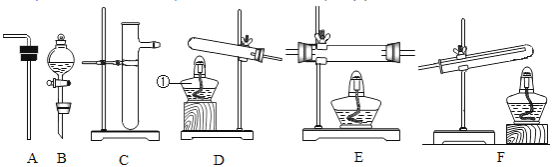
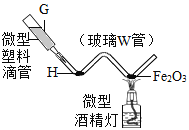
(一)利用图装置回答问题(假设赤铁矿粉样品中的Fe2O3完全反应,赤铁矿中杂质不参与反应):
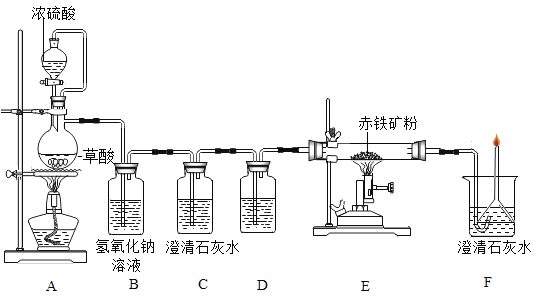
(1)A装置的作用是制取一氧化碳,反应的化学方程式为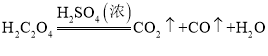 。根据反应装置判断,化学方程式中还缺少的条件是___________________。
。根据反应装置判断,化学方程式中还缺少的条件是___________________。
(2)C装置的作用是______,D装置中药品的名称是________,E装置中发生反应的化学方程式为________,F处将尾气燃烧掉的目的是______。
(3)实验中记录的数据如下表,据此计算赤铁矿中氧化铁的质量分数为________。
玻璃管质量 | 玻璃管和药品反应前质量 | 玻璃管和药品反应后质量 |
65.6g | 75.6g | 73.2g |
(4)有同学提出可以根据F装置中增加的质量来计算赤铁矿中氧化铁的质量,你同意此看法吗?
说出你的观点和理由是_______。
(二)利用图装置进行甲、乙对比实验,探究温度对CO和Fe2O3反应的影响(固定装置和尾气处理装置略,所用固体药品为纯净物)。
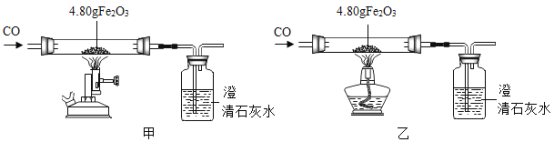
(1)反应过程中观察到,甲、乙两组的澄清石灰水均变浑浊,集气瓶中发生反应的化学方程式为________。
(2)完全反应后,甲、乙两组的生成物均为黑色粉末,分别用两组的生成物进行以下实验:
步骤 | 操作 | 甲组现象 | 乙组现象 |
1 | 称量黑色粉末质量/g | m1 | m2 |
2 | 取黑色粉末,用磁铁吸引 | 全部被吸引 | 全部被吸引 |
3 | 取黑色粉末,加入足量CuSO4溶液 | 黑色粉末溶解,有红色物质生成 | 无明显现象 |
(注:铁的氧化物中,只有Fe3O4能被磁铁吸引)
①甲组的黑色粉末与CuSO4溶液反应的化学方程式是_____。
②小明同学查阅资料后发现Fe3O4在常温下不与CuSO4溶液反应,故猜想乙组的生成物为Fe3O4。
小丽提出不同意见:假设乙组黑色粉末中除了有Fe3O4,还可能含有少量铁粉,铁粉的含量低,与硫酸铜溶液反应也可能无明显现象。
了进一步确定乙组生成物成分,小组同学提出,如果m2恰好为______________g,则小明的猜想正确,如果m2_____________________(填“大于”或“小于”)该质量,则乙组生成物中还含有少量铁粉。