题目内容
为了测定某铜锌合金的组成,某校化学课外活动小组利用该合金粉末与稀硫酸反应,进行了三次实验,所得相关的实验数据记录如下:
| 第一次 | 第二次 | 第三次 | |
| 所取合金的质量/g | 10 | 10 | 20 |
| 所用稀硫酸的质量/g | 50 | 80 | 50 |
| 生成氢气的质量/g | 0.2 | 0.2 | 0.2 |
(2)从上表数据分析,当所取合金与所用稀硫酸的质量比为________时,表明合金中的锌与稀硫酸恰好完全反应.(提示:铜与稀硫酸不反应)
(3)试计算该铜锌合金中锌的质量分数.
(4)计算当所用合金与稀硫酸恰好完全反应时,所得溶液中溶质的质量分数.
解:(1)Zn+H2SO4→ZnSO4+H2↑;
(2)由于合金中的锌与稀硫酸恰好完全反应所取合金与所用稀硫酸分别为10g,50g,故其质量比为1:5;
故答案为:1:5.
(3)设合金中锌的质量为x,生成硫酸锌质量为y.
Zn+H2SO4→ZnSO4+H2↑
65 161 2
x y 0.2g
∴x:65=0.2g:2,
解之得:x=6.5g,
该铜锌合金中锌的质量分数为: ×100%=65%;
×100%=65%;
(4)y:161=0.2g:2,
解之得:y=16.1g,
所得溶液中ZnSO4的质量分数: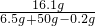 ×100%=28.6%.
×100%=28.6%.
答:(3)该铜锌合金中锌的质量分数为65%;
(4)所得溶液中ZnSO4的质量分数为28.6%.
分析:(1)由于铜与稀硫酸不反应,故铜锌合金与稀硫酸的反应,为锌与稀硫酸的反应,可直接写出反应方程式;
(2)从三次实验数据可知,第一、第二次反应中稀硫酸过量,第三次反应中锌过量,又因为第三次反应中硫酸产生的氢气恰好为0.2g,所以第一次反应中合金中的锌与稀硫酸恰好完全反应,从而得出它们的质量比.
(3)根据第一次实验产生氢气的质量和其所取用的稀硫酸与合金样品的质量,可求出合金中锌的质量;
(4)根据(3)中化学方程式的比例关系,求出溶质的质量,及溶液的总量,代入公式可以求出恰好完全反应后所得溶液中溶质的质量分数.
点评:本题是借助于数学模型,利用图表的方式来分析和解决化学计算中的有关问题,要求学生有较强的识图能力和数据分析能力.
(2)由于合金中的锌与稀硫酸恰好完全反应所取合金与所用稀硫酸分别为10g,50g,故其质量比为1:5;
故答案为:1:5.
(3)设合金中锌的质量为x,生成硫酸锌质量为y.
Zn+H2SO4→ZnSO4+H2↑
65 161 2
x y 0.2g
∴x:65=0.2g:2,
解之得:x=6.5g,
该铜锌合金中锌的质量分数为:
 ×100%=65%;
×100%=65%;(4)y:161=0.2g:2,
解之得:y=16.1g,
所得溶液中ZnSO4的质量分数:
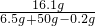 ×100%=28.6%.
×100%=28.6%.答:(3)该铜锌合金中锌的质量分数为65%;
(4)所得溶液中ZnSO4的质量分数为28.6%.
分析:(1)由于铜与稀硫酸不反应,故铜锌合金与稀硫酸的反应,为锌与稀硫酸的反应,可直接写出反应方程式;
(2)从三次实验数据可知,第一、第二次反应中稀硫酸过量,第三次反应中锌过量,又因为第三次反应中硫酸产生的氢气恰好为0.2g,所以第一次反应中合金中的锌与稀硫酸恰好完全反应,从而得出它们的质量比.
(3)根据第一次实验产生氢气的质量和其所取用的稀硫酸与合金样品的质量,可求出合金中锌的质量;
(4)根据(3)中化学方程式的比例关系,求出溶质的质量,及溶液的总量,代入公式可以求出恰好完全反应后所得溶液中溶质的质量分数.
点评:本题是借助于数学模型,利用图表的方式来分析和解决化学计算中的有关问题,要求学生有较强的识图能力和数据分析能力.

练习册系列答案
 特高级教师点拨系列答案
特高级教师点拨系列答案
相关题目
为了测定某铜锌合金的组成,王华称取10g该合金粉末,在粉末中连续三次加入稀盐酸反应.每加一次盐酸,王华记录所得气体的质量,测得实验数据如下:
求出该合金中铜的质量分数.
| 第一次 | 第二次 | 第三次 | |
| 连续加入盐酸的体积(ml) | 10 | 10 | 10 |
| 生成氢气的质量(g) | 0.08 | 0.08 | 0.04 |
为了测定某铜锌合金的组成,某校化学课外活动小组利用该合金粉末与稀硫酸反应,进行了三次实验,所得相关的实验数据记录如下:
(1)试计算该铜锌合金中含锌的质量分数.
(2)所用合金与稀硫酸恰好完全反应时所得溶液中溶质的质量分数.
| 第一次 | 第二次 | 第三次 | |
| 所取合金的质量/g | 10 | 10 | 20 |
| 所用稀硫酸的质量/g | 50 | 80 | 50 |
| 生成氢气的质量/g | 0.2 | 0.2 | 0.2 |
(2)所用合金与稀硫酸恰好完全反应时所得溶液中溶质的质量分数.
 (2013?浦口区一模)Cu与Zn的合金称为黄铜,有优良的导热性和耐腐蚀性,可用作各种仪器零件.
(2013?浦口区一模)Cu与Zn的合金称为黄铜,有优良的导热性和耐腐蚀性,可用作各种仪器零件.