题目内容
【题目】为探究碳还原氧化铜的最佳实验条件,用木炭粉和氧化铜的干燥混合物1~2.5g进行系列实验。
(查阅资料)碳还原氧化铜得到的铜中可能含有少量的氧化亚铜;铜不能与稀硫酸反应。氧化亚铜为红色固体,能与稀硫酸反应:Cu2O+H2SO4═CuSO4+H2O+Cu。
(进行实验)实验1:取质量比1:11的木炭粉和氧化铜混合物1.3g,进行实验。
序号 | 1﹣1 | 1﹣2 |
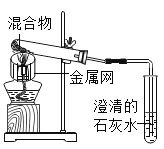
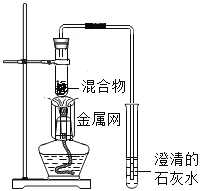
装置 |
|
|
反应后物质的颜色、状态 | 黑色粉末中混有少量红色固体 | 红色固体有金属光泽,混有极少量黑色物质 |
实验2:取一定量的混合物,用1﹣2装置进行实验。
序号 | 木炭粉与氧化铜的质量比 | 反应后物质的颜色、状态 | |
2﹣1 | 1:9 | 红色固体有金属光泽 | 混有少量黑色物质 |
2﹣2 | 1:10 | 混有很少量黑色物质 | |
2﹣3 | 1:11 | 混有极少量黑色物质 | |
2﹣4 | 1:12 | 无黑色物质 | |
2﹣5 | 1:13 | 混有较多黑色物质 | |
(解释与结论)
(1)氧化铜是_____色固体。
(2)①配平化学方程式:C+_____CuO![]() _____Cu+____CO2↑。
_____Cu+____CO2↑。
②该反应前后化合价发生改变的元素是:_______。
(3)实验1﹣2中,证明产生了CO2的现象是_____。
(4)实验1的目的是_____。
(5)实验2的结论是_____。
(反思与评价)
(6)实验2没有进行质量比为1:14的实验,理由是_____。
(7)为检验2﹣4的红色固体中是否含Cu2O,所需试剂是_____。
【答案】黑 2 2 1 C、Cu 澄清石灰水变浑浊 探究氧化铜与木炭的不同加热方式(角度、条件)对其反应的影响 木炭与氧化铜质量比为1:12时恰好完全反应,因此木炭与氧化铜反应的最佳质量比为1:12 木炭与氧化铜的质量比为1:13时,氧化铜已过量 稀硫酸
【解析】
(1)氧化铜是黑色固体。
(2)由质量守恒定律可知,碳与氧化铜高温条件下反应产生铜和二氧化碳的化学方程式:C+2CuO![]() 2Cu+CO2↑。
2Cu+CO2↑。
②该反应前后碳有0价变为+4价,铜由+2价变为0价,化合价发生改变的元素是:碳元素和铜元素;
(3)实验1﹣2中,二氧化碳与澄清的石灰水反应产生碳酸钙沉淀,证明产生了CO2的现象是:澄清的石灰水变浑浊;
(4)实验1中:试管口略微向下与试管口垂直向上对比,其目的是:探究氧化铜与木炭的不同加热方式(角度或条件)对其反应结果的影响;
(5)实验2中,采用多次不同比例的碳粉与氧化铜反应,无黑色物质,结论是:木炭与氧化铜质量比为1:12时恰好完全反应;因此木炭与氧化铜反应的最佳质量比为1:12 ;
(6)实验2没有进行质量比为1:14的实验,理由是:木炭与氧化铜的质量比为1:13时,氧化铜已过量,不需要增大比例再次实验;
(7)铜不能与稀硫酸反应,但氧化亚铜为红色固体,能与稀硫酸反应产生硫酸铜蓝色溶液,为检验2﹣4的红色固体中是否含Cu2O,所需试剂是:稀硫酸,将稀硫酸与红色固体混合反应后,观察溶液是否变蓝。