题目内容
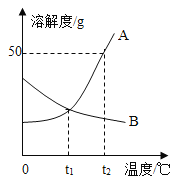
【题目】如图为Na2Cr2O7、Na2SO4两种物质的溶解度曲线,下列说法正确的是( )
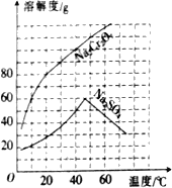
A.60℃时两种物质的溶解度:Na2Cr2O7大于Na2SO4
B.20℃时,Na2Cr2O7饱和溶液中溶质的质量分数为80%
C.两种物质的溶解度都随温度的升高而增大
D.50℃时,将210gNa2Cr2O7饱和溶液降温到10℃,析出150g Na2Cr2O7
【答案】A
【解析】
解:A、通过分析溶解度曲线可知,60℃时两种物质的溶解度:Na2Cr2O7大于Na2SO4;故选项正确;
B、20℃时,Na2Cr2O7的溶解度是80g,所以饱和溶液中溶质的质量分数为![]() ×100%≠80%;故选项错误;
×100%≠80%;故选项错误;
C、大于48℃时,硫酸钠的溶解度逐渐减小;故选项错误;
D、50℃时,Na2Cr2O7的溶解度是110g,10℃时,Na2Cr2O7的溶解度是60g,将210gNa2Cr2O7饱和溶液降温到10℃,析出50g Na2Cr2O7;故选项错误。
故选:A。

 每日10分钟口算心算速算天天练系列答案
每日10分钟口算心算速算天天练系列答案【题目】为探究碳还原氧化铜的最佳实验条件,用木炭粉和氧化铜的干燥混合物1~2.5g进行系列实验。
(查阅资料)碳还原氧化铜得到的铜中可能含有少量的氧化亚铜;铜不能与稀硫酸反应。氧化亚铜为红色固体,能与稀硫酸反应:Cu2O+H2SO4═CuSO4+H2O+Cu。
(进行实验)实验1:取质量比1:11的木炭粉和氧化铜混合物1.3g,进行实验。
序号 | 1﹣1 | 1﹣2 |
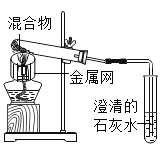
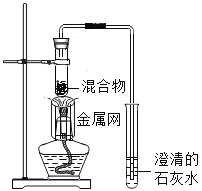
装置 |
|
|
反应后物质的颜色、状态 | 黑色粉末中混有少量红色固体 | 红色固体有金属光泽,混有极少量黑色物质 |
实验2:取一定量的混合物,用1﹣2装置进行实验。
序号 | 木炭粉与氧化铜的质量比 | 反应后物质的颜色、状态 | |
2﹣1 | 1:9 | 红色固体有金属光泽 | 混有少量黑色物质 |
2﹣2 | 1:10 | 混有很少量黑色物质 | |
2﹣3 | 1:11 | 混有极少量黑色物质 | |
2﹣4 | 1:12 | 无黑色物质 | |
2﹣5 | 1:13 | 混有较多黑色物质 | |
(解释与结论)
(1)氧化铜是_____色固体。
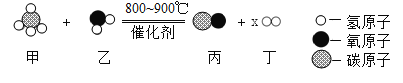
(2)①配平化学方程式:C+_____CuO![]() _____Cu+____CO2↑。
_____Cu+____CO2↑。
②该反应前后化合价发生改变的元素是:_______。
(3)实验1﹣2中,证明产生了CO2的现象是_____。
(4)实验1的目的是_____。
(5)实验2的结论是_____。
(反思与评价)
(6)实验2没有进行质量比为1:14的实验,理由是_____。
(7)为检验2﹣4的红色固体中是否含Cu2O,所需试剂是_____。