题目内容
【题目】用图装置进行空气中氧气含量测定的实验。
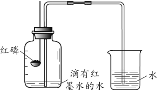
(1)证明空气中氧气含量约为1/5的实验现象是______。
(2)实验中观察到烧杯中的水变为红色,原因是______。
【答案】瓶中的液面上升了约1/5 红磷燃烧放热,使瓶内压强增大,水流到烧杯中
【解析】
磷燃烧能够消耗空气中的氧气,氧气消耗后,容器中的气压减小,在外界大气压作用下,水进入容器,进入容器中的水的体积即为容器内空气中的氧气体积。
(1)红磷燃烧耗尽了装置内的氧气,由于氧气约占空气体积的五分之一,所以装置冷却至室温后,瓶内瓶中的液面上升了约1/5,进入的水的体积即为消耗的氧气的体积,说明空气中氧气含量约为1/5。
(2)红磷燃烧放热,使瓶内压强增大,水流到烧杯中,所以实验中观察到烧杯中的水变为红色。

 期末冲刺100分创新金卷完全试卷系列答案
期末冲刺100分创新金卷完全试卷系列答案【题目】为探究碳还原氧化铜的最佳实验条件,用木炭粉和氧化铜的干燥混合物1~2.5g进行系列实验。
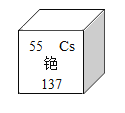
(查阅资料)碳还原氧化铜得到的铜中可能含有少量的氧化亚铜;铜不能与稀硫酸反应。氧化亚铜为红色固体,能与稀硫酸反应:Cu2O+H2SO4═CuSO4+H2O+Cu。
(进行实验)实验1:取质量比1:11的木炭粉和氧化铜混合物1.3g,进行实验。
序号 | 1﹣1 | 1﹣2 |
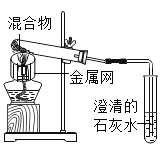
装置 |
|
|
反应后物质的颜色、状态 | 黑色粉末中混有少量红色固体 | 红色固体有金属光泽,混有极少量黑色物质 |
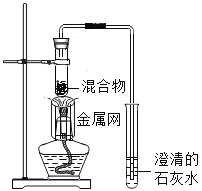
实验2:取一定量的混合物,用1﹣2装置进行实验。
序号 | 木炭粉与氧化铜的质量比 | 反应后物质的颜色、状态 | |
2﹣1 | 1:9 | 红色固体有金属光泽 | 混有少量黑色物质 |
2﹣2 | 1:10 | 混有很少量黑色物质 | |
2﹣3 | 1:11 | 混有极少量黑色物质 | |
2﹣4 | 1:12 | 无黑色物质 | |
2﹣5 | 1:13 | 混有较多黑色物质 | |
(解释与结论)
(1)氧化铜是_____色固体。
(2)①配平化学方程式:C+_____CuO![]() _____Cu+____CO2↑。
_____Cu+____CO2↑。
②该反应前后化合价发生改变的元素是:_______。
(3)实验1﹣2中,证明产生了CO2的现象是_____。
(4)实验1的目的是_____。
(5)实验2的结论是_____。
(反思与评价)
(6)实验2没有进行质量比为1:14的实验,理由是_____。
(7)为检验2﹣4的红色固体中是否含Cu2O,所需试剂是_____。