题目内容
 复习时,课堂上老师引导我们回顾了二个探究实验.
复习时,课堂上老师引导我们回顾了二个探究实验.
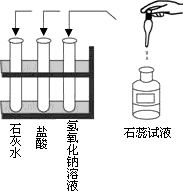
探究1:在实验室做酸和碱与指示剂反应的实验,所用试剂如图所示,实验后把废液集中倒入废液缸中.
(1)废液呈红色,说明废液显________性;
(2)写出废液中所含溶质的化学式________.
探究2:某学习小组的三位同学为了测定H2SO4与NaOH发生中和反应时放出的热量,他们在下图所示的小烧杯中装入一定量的NaOH溶液,测其温度;另取一定量的硫酸溶液,测其温度后,再缓缓地倾入小烧杯中,并边加边用环形玻璃棒上下移动搅拌,记录溶液温度的变化.甲、乙、丙三位同学实验时选择的试剂情况见表:
| 使用的NaOH情况 | 使用的H2SO 4情况 | |
| 甲 | NaOH固体 | 稀H 2SO 4 |
| 乙 | NaOH稀溶液 | 浓H2SO4 |
| 丙 | NaOH稀溶液 | 稀H2SO4 |
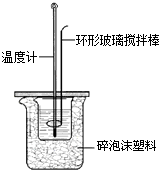
①玻璃棒下端为什么要做成环形?________;
②碎泡沫塑料的作用是什么?________.
(2)甲、乙、丙三位同学中,有两位同学选择的试剂有错误.从溶液温度改变的因素
考虑,指出错误的原因是:
①同学错误的原因是________;
②同学错误的原因是________.
(3)另一位回学选择的试剂正确,但用上述实验方法测得的中和热数值都会偏小,试分析可能造成误差的原因:________.
解:探究1:(1)石蕊遇酸变红,废液呈红色,说明废液呈酸性,所以本题答案为:酸性;
(2)石灰水与盐酸反应生成氯化钙和水,氢氧化钠与盐酸反应生成氯化钠和水,废液呈酸性,说明一定含盐酸,所以本题答案为:NaCl、CaCl2、HCl;
探究2:(1)①要使氢氧化钠与稀硫酸充分反应,需要不断搅拌,因为用到温度计测定,为防止碰坏温度计,所以可上下搅动,普通玻璃棒的搅拌效果不明显,做成环形易于搅拌,所以本题答案为:便于玻璃棒上下移动就能搅拌溶液,防止破坏温度计;
②为保证实验结果的客观准确性,需防止热量散失,而泡沫塑料具有隔热的作用,所以本题答案为:隔热,防止热量散失;
(2)①氢氧化钠固体溶于水会放热,无法确定热量的变化是反应放出的还是氢氧化钠固体溶于水放出的,对实验结果有干扰,所以本题答案为:NaOH固体溶于水会放热,影响反应热的测定;
②浓硫酸溶于水会放出热量,无法确定热量的变化是反应放出的还是浓硫酸溶于水放出的,对实验结果有干扰,所以本题答案为:浓H2SO4溶于水会放热,影响反应热的测定;
③用上述实验方法测得的中和热数值都会偏小,说明反应过程中有热量的散失,造成热量散失的原因可能与仪器装置有关,也可能与反应物的量有关,所以本题答案为:小烧杯未加盖,热量散失或反应物量太少(其他合理答案均可).
分析:石灰水与盐酸反应生成氯化钙和水,氢氧化钠与盐酸反应生成氯化钠和水,石蕊遇酸变红,遇碱变蓝;氢氧化钠与稀硫酸的中和反应要放出热量,要设计实验证明,需排除干扰因素,氢氧化钠固体和浓硫酸溶于水都会放出热量,另外要注意减小实验误差,即实验过程中减少热量的放出.
点评:本题考查了实验方案的设计对实验结果的影响,在进行实验设计时,要注意某些变量的控制,同时需考虑药品的选择、仪器装置的选择对实验结果的影响.
(2)石灰水与盐酸反应生成氯化钙和水,氢氧化钠与盐酸反应生成氯化钠和水,废液呈酸性,说明一定含盐酸,所以本题答案为:NaCl、CaCl2、HCl;
探究2:(1)①要使氢氧化钠与稀硫酸充分反应,需要不断搅拌,因为用到温度计测定,为防止碰坏温度计,所以可上下搅动,普通玻璃棒的搅拌效果不明显,做成环形易于搅拌,所以本题答案为:便于玻璃棒上下移动就能搅拌溶液,防止破坏温度计;
②为保证实验结果的客观准确性,需防止热量散失,而泡沫塑料具有隔热的作用,所以本题答案为:隔热,防止热量散失;
(2)①氢氧化钠固体溶于水会放热,无法确定热量的变化是反应放出的还是氢氧化钠固体溶于水放出的,对实验结果有干扰,所以本题答案为:NaOH固体溶于水会放热,影响反应热的测定;
②浓硫酸溶于水会放出热量,无法确定热量的变化是反应放出的还是浓硫酸溶于水放出的,对实验结果有干扰,所以本题答案为:浓H2SO4溶于水会放热,影响反应热的测定;
③用上述实验方法测得的中和热数值都会偏小,说明反应过程中有热量的散失,造成热量散失的原因可能与仪器装置有关,也可能与反应物的量有关,所以本题答案为:小烧杯未加盖,热量散失或反应物量太少(其他合理答案均可).
分析:石灰水与盐酸反应生成氯化钙和水,氢氧化钠与盐酸反应生成氯化钠和水,石蕊遇酸变红,遇碱变蓝;氢氧化钠与稀硫酸的中和反应要放出热量,要设计实验证明,需排除干扰因素,氢氧化钠固体和浓硫酸溶于水都会放出热量,另外要注意减小实验误差,即实验过程中减少热量的放出.
点评:本题考查了实验方案的设计对实验结果的影响,在进行实验设计时,要注意某些变量的控制,同时需考虑药品的选择、仪器装置的选择对实验结果的影响.

练习册系列答案
相关题目
复习时,常用专题的探究的方法学习常见物质的组成、性质与制取,课堂上老师引导我们回顾了几个探究实验.
(1)探究1:研究常见物质性质-氢氧化钠与盐酸是否刚好完全中和.
①探索:用玻璃棒蘸取反应后的溶液滴在pH试纸上,发现pH<7,说明盐酸过量.
②验证:
写出②中涉及的化学方程式
(2)探究2:研究常见物质的制取-制取氢氧化钠溶液.
甲同学向盛有澄清石灰水的烧杯中加入过量的碳酸钠溶液,生成白色沉淀,过滤后得到无色溶液,他说:“我制得了氢氧化钠溶液!”
乙同学却说:“这种无色溶液不一定含有氢氧化钠”他提出了如下实验:
丙同学认为乙同学实验方案也不够严密,不能证明无色溶液中一定含有氢氧化钠,理由是 .
丙同学设计了另一个实验:
我认为:乙同学和丙同学的实验是为了验证甲同学结论的可靠性,甲同学的结论不可靠,原因是 ,显然丙同学的实验可靠性比乙同学的实验好,原因是 .
(3)经过实验发现,某同学取53g 10%的碳酸钠溶液与152g饱和澄清石灰水恰好完全反应,求反应后溶液中溶质的质量分数.
(1)探究1:研究常见物质性质-氢氧化钠与盐酸是否刚好完全中和.
①探索:用玻璃棒蘸取反应后的溶液滴在pH试纸上,发现pH<7,说明盐酸过量.
②验证:
| 实验内容 | 实验现象 | 解释与结论 |
| 取少量溶液于试管中, | 证明研究结论正确 |
(2)探究2:研究常见物质的制取-制取氢氧化钠溶液.
甲同学向盛有澄清石灰水的烧杯中加入过量的碳酸钠溶液,生成白色沉淀,过滤后得到无色溶液,他说:“我制得了氢氧化钠溶液!”
乙同学却说:“这种无色溶液不一定含有氢氧化钠”他提出了如下实验:
| 实验内容 | 实验现象 | 实验结论 |
| 用试管取无色溶液少许,滴入2滴酚酞试液 | 无色酚酞变红 | 无色溶液中有氢氧化钠 |
丙同学设计了另一个实验:
| 实验步骤 | 实验现象 | 实验结论 |
| 无色溶液中确实含有氢氧化钠 |
(3)经过实验发现,某同学取53g 10%的碳酸钠溶液与152g饱和澄清石灰水恰好完全反应,求反应后溶液中溶质的质量分数.
复习时,常用专题探究的方法学习常见物质的组成、性质与制取,课堂上老师引导我们回顾了几探究实验.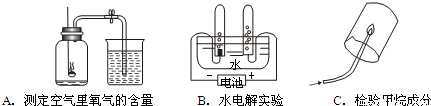
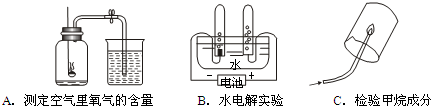
探究1:研究常见物质组成.
A、B、C都是研究物质组成的实验.从研究方法可知,A实验是利用可燃物消耗瓶内的______,使瓶内压强减小来推测空气里氧气含量的.B实验是通过证明生成物的______ 来推断水的组成的.而C实验与______(填实验代号)实验的方法相同.
探究2:研究常见物质性质--氢氧化钠与硫酸是否刚好完全中和.
(1)探索:用玻璃棒蘸取反应后的溶液滴在pH试纸上,发现该溶液的pH<7,说明硫酸过量.
(2)验证:
写出(2)出中涉及的化学方程式______.
探究3:研究常见物质制取--制取氢氧化钠溶液.
小京同学向盛有澄清石灰水的烧杯中加入一定量的碳酸钠溶液,生成白色沉淀,过滤后得到无色溶液,他说:“我制得了氢氧化钠溶液!”
小欢同学却说:“这种无色溶液不一定就是氢氧化钠.”
根据小欢同学的质疑,你认为所得溶液中还可能含有______或______.
请你设计实验证明所得溶液中只有含氢氧化钠.

探究1:研究常见物质组成.
A、B、C都是研究物质组成的实验.从研究方法可知,A实验是利用可燃物消耗瓶内的______,使瓶内压强减小来推测空气里氧气含量的.B实验是通过证明生成物的______ 来推断水的组成的.而C实验与______(填实验代号)实验的方法相同.
探究2:研究常见物质性质--氢氧化钠与硫酸是否刚好完全中和.
(1)探索:用玻璃棒蘸取反应后的溶液滴在pH试纸上,发现该溶液的pH<7,说明硫酸过量.
(2)验证:
| 实验内容 | 实验现象 | 解释与结论 |
| 取反应后少量溶液于试管中, ______. | ______ | 证明硫酸过量 |
探究3:研究常见物质制取--制取氢氧化钠溶液.
小京同学向盛有澄清石灰水的烧杯中加入一定量的碳酸钠溶液,生成白色沉淀,过滤后得到无色溶液,他说:“我制得了氢氧化钠溶液!”
小欢同学却说:“这种无色溶液不一定就是氢氧化钠.”
根据小欢同学的质疑,你认为所得溶液中还可能含有______或______.
请你设计实验证明所得溶液中只有含氢氧化钠.
| 实验步骤 | 实验现象 | 实验结论 |
| ______ | ______ | ______ |