题目内容
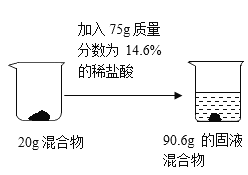
【题目】为测定某碳酸钙样品中碳酸钙的质量分数,某学习小组进行了如下实验探究。取10g碳酸钙样品放入烧杯中,加入稀盐酸至不再产生气泡为止(样品中的杂质仅有 CaCl2),并绘制了加入稀盐酸的质量与放出气体质量的坐标图(如图).

(1)所用稀盐酸的溶质质量分数是多少?______
(2)该样品中碳酸钙的质量分数为多少?______
(3)当盐酸和样品恰好完全反应,所得溶液中溶质质量分数是多少?(规范写出计算过程)______
【答案】6.9% 80% 12.0%
【解析】
由题意碳酸钙与稀盐酸反应生成二氧化碳的质量为3.52g,设反应消耗的HCl质量为x,参加反应的CaCO3的质量为y,反应生成的CaCl2质量为z,则有:
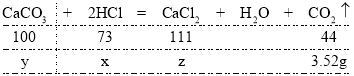
由![]() 解得x=5.84g
解得x=5.84g
由![]() 解得y=8g
解得y=8g
由![]() 解得z=8.88g
解得z=8.88g
(1)所用稀盐酸的溶质质量分数为![]()
(2)样品中CaCO3的质量分数为![]()
(3)样品中所含氯化钙的质量为10g-8g=2g,反应后的溶液溶质质量分数为![]()
答:(1)稀盐酸的溶质质量分数为6.9%。
(2)样品中CaCO3的质量分数为80%。
(3)反应后的溶液溶质质量分数为12.0%。

练习册系列答案
 励耘书业暑假衔接宁波出版社系列答案
励耘书业暑假衔接宁波出版社系列答案
相关题目
【题目】KCl与KNO3在不同温度的溶解度数据如表。则下列说法正确的是( )
温度/℃ | 10 | 20 | 30 | 40 | 50 |
KCl | 30g | 33g | 35g | 38g | 41g |
KNO3 | 21g | 31g | 45g | 65g | 88g |
A.KNO3溶解度大于KCl的溶解度
B.两物质溶解度相等的温度在10-20℃之间
C.在30℃时,5gKNO3加入到10g水中可得到33.3%的KNO3溶液
D.在50℃时,两物质各10g分别加入20g水中,充分溶解,只有KCl中有固体剩余