题目内容
【题目】化学是在分子、原子层次上研究物质的科学。

(1)构成物质的粒子有分子、原子和____________。
(2)图为三种元素的原子结构示意图。氧原子在化学反应中容易____________电子(填“得到”或“失去”)。
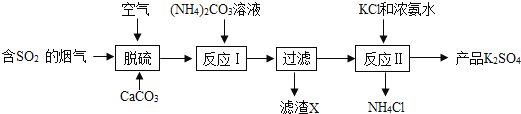
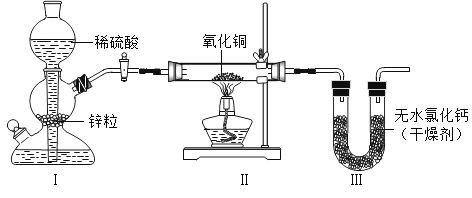
(3)二氧化硫和二氧化碳都能与氢氧化钠溶液反应生成盐和水。将二氧化硫气体通入氢氧化钠溶液中生成亚硫酸钠和水,写出该反应的化学方程式______________。
(4)硒元素与氧、硫元素的化学性质相似,原因是它们原子的______________相同。
(5)硒元素能增强人体免疫力,延缓衰老,山药等食物中富含硒元素。硒(Se)在氧气中燃烧生成二氧化硒。写出硒在氧气中燃烧反应的化学方程式_________________。
【答案】离子 得到 SO2+2NaOH=Na2SO3+H2O 最外层电子数 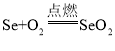
【解析】
(1)像碳、铁、氦气等物质是由原子构成的。像二氧化碳、水、甲烷等物质是由分子构成的。像氯化钠是由离子构成的物质。故答案为:离子;
(2)图3的原子的最外层电子数为6,在化学反应中,易得到2个电子形成8电子的稳定结构。故答案为:得到;
(3)二氧化硫和氢氧化钠反应生成亚硫酸钠和水,亚硫酸根为:SO32-。故答案为:SO2+2NaOH=Na2SO3+H2O;
(4)硒元素、氧元素、硫元素的化学性质相似,是因为三种元素的原子的最外层电子数相同。故答案为:最外层电子数;
(5)硒在氧气中燃烧生成二氧化硒,则生成物的化学式为SeO2。则该反应的化学反应方程式为: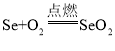 。故答案为:
。故答案为: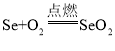

【题目】元素周期表中,同周期元素的结构和性质呈现一定的规律性变化。下表列出的是第三周期元素的原子半径及主要化合价(部分信息未列出)。下列有关说法不正确的是( )
元素 | Na | Mg | ① | Si | P | ② | Cl |
原子的最外层电子数 | 1 | 2 | 3 | 4 | 5 | 6 | 7 |
原子半径(10-10m) | 1.86 | 1.60 | 1.43 | ③ | 1.10 | 10.2 | 0.994 |
最高正价最低负价 | +1 | +2 | ④ | +4 -4 | +5 -3 | ⑤ | +7-1 |
A.⑤处的最高正价是+6,最低负价是-2
B.元素①的原子序数是 13,①和②形成的化合物的化学式为 AlS
C.第三周期元素(Na→Cl)的最高正价数等于其原子的最外层电子数
D.③处的数值介于 1.10~1.43 之间