题目内容
【题目】海水中有大量可以利用的化学资源,例如氯化镁、氯化钠、溴化钾等,综合利用海水制备金属镁的流程如图所示:
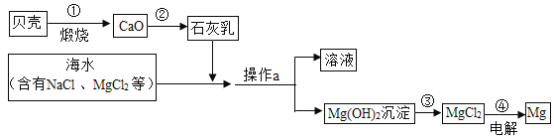
(1)通过操作a后所得溶液中的溶质肯定含有___________。
(2)工业上冶炼镁常用第④步反应,已知电解熔融MgCl2产生Mg和Cl2 (氯气),则反应的化学方程式为___________。若得氢氧化镁5.8t, 理论上能制得镁___________t;
(3)上述①②③④四步反应涉及到___________种基本反应类型。
【答案】氯化钠和氯化钙 MgCl2![]() Mg+Cl2↑ 2.4 三
Mg+Cl2↑ 2.4 三
【解析】
(1)石灰乳与氯化镁反应生成氢氧化镁沉淀和氯化钙,石灰乳与氯化钠不反应,操作a后所得溶液中的溶质肯定含有氯化钠和氯化钙;故填:氯化钠和氯化钙;
(2)电解熔融MgCl2产生Mg和Cl2 (氯气),则反应的化学方程式为MgCl2![]() Mg+Cl2↑;
Mg+Cl2↑;
设得氢氧化镁5.8t,理论上能制得镁的质量为:5.8t×![]() =2.4t。故填:MgCl2
=2.4t。故填:MgCl2![]() Mg+Cl2↑;2.4;
Mg+Cl2↑;2.4;
(3)①贝壳煅烧制取氧化钙是碳酸钙受热分解生成氧化钙和二氧化碳的反应,属于分解反应;②氧化钙与水反应生成氢氧化钙,反应物有两种,生成物为一种,为化合反应;③氢氧化镁与盐酸反应为复分解反应;④氯化镁通电为分解反应。故整个流程中涉及到分解、化合、复分解三种基本反映类型;故填:三。

 名校课堂系列答案
名校课堂系列答案【题目】为测定某黄铜(铜锌合金)样品中铜的含量,某化学活动小组分三次进行实验,实验数据如表,请回答下列问题:
所取药品 | 第一次 | 第二次 | 第三次 |
黄铜样品质量(g) | 12 | 10 | 10 |
稀盐酸质量(g) | 100 | 100 | 150 |
生成气体质量(g) | 0.2 | 0.2 | 0.2 |
(1)第____次实验中,药品成分恰好完全反应。
(2)黄铜样品中铜的质量分数是多少?恰好完全反应时所得溶液的溶质质量分数是多少________?(精确到0.1%)