题目内容
【题目】工业合成氨与制备硝酸可联合生产,流程示意图如下。
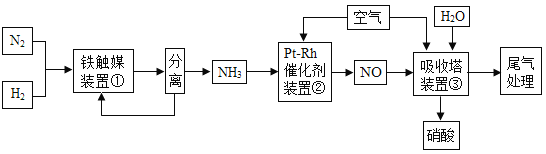
请回答下列问题:
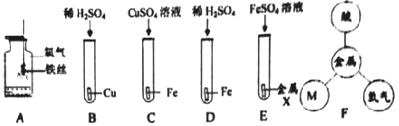
(1)![]() 、
、![]() 进入装置①中,在高温、高压以及催化剂条件下合成氨气,该反应的化学方程式为_____。
进入装置①中,在高温、高压以及催化剂条件下合成氨气,该反应的化学方程式为_____。
(2)装置②中的反应机理如下图。结合该图说明催化剂的作用及其在化学反应前后的情况分别是_____,_____。

(3)NO和![]() 进入装置③,被
进入装置③,被![]() 吸收生成硝酸,该反应的化学方程式为_____。
吸收生成硝酸,该反应的化学方程式为_____。
(4)该流程排放的尾气含有氮的氧化物,若直接排放,会带来的环境污染有_____(写一条)。
【答案】 改变化学反应速率 本身的质量和化学性质都没有发生变化
改变化学反应速率 本身的质量和化学性质都没有发生变化 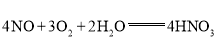 酸雨(或“光化学烟雾”)
酸雨(或“光化学烟雾”)
【解析】
(1)工业上可以由N2和H2在高温高压以及催化剂的条件下合成![]() ,即
,即 ;
;
(2)结合该图可知催化剂的作用是改变化学反应速率,催化剂在化学反应前后本身的质量和化学性质都没有发生变化;
(3)一氧化氮和氧气及水反应生成硝酸,化学方程式为:![]() ;
;
(4)氮的氧化物,若直接排放,会造成空气的污染,形成酸雨。

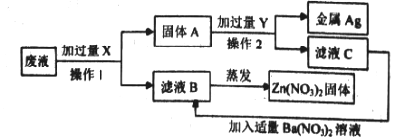
【题目】一天,实验助手小娟走进实验室和老师一起检查每个实验桌上的药品、仪器是否齐备,走到某组的时候,看到了一个不和谐的“音符”(如图).
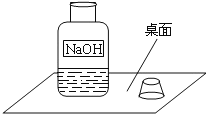
(1)此情此景你首先想到的是它可能变质了,写出该变质反应的化学方程式:__________________
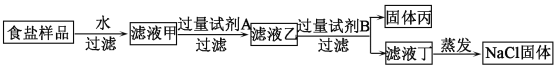
(2)围绕此瓶NaOH溶液是否变质的问题,小娟利用实验室的三种试剂(氯化钙溶液、稀盐酸、酚酞试液)展开了探究活动。
①取少量溶液于试管中,滴加某种试剂,有气泡产生,由此证明NaOH溶液已经变质。你认为小娟所加的试剂是_____________。
②欲证明变质的溶液中尚存NaOH,请你帮助小娟完成以下探究方案:
探究目的 | 探究步骤 | 预计现象 |
除尽溶液中的CO32- | a取少量溶液于试管中,滴加足量的_______试剂 | 有白色沉淀产生 |
证明溶液中尚存NaOH | b向实验①所得溶液中滴加酚酞试液 | ___________ |
(3)通过上述探究,说明氢氧化钠溶液暴露在空气中与________反应变质,故应该________保存。