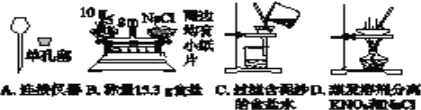��Ŀ����
����Ŀ�������ģ�ij������Ȥ��ͬѧ��ͼ��ʵ��װ�ý�������ʵ�顣���Լ������������������Ӧ����ȫ��װ�ÿ��ظ�ʹ�ã����ּг�װ����ʡ�ԣ����װ�����������á���
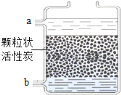
��̽��һ������ͬѧ����Aװ���Ʊ�O2���������Ƶõ�O2��֤B�еĺ�ɫ��ĩ�Ƿ�̿�ۡ�
��1��A�з�Ӧ�Ļ�ѧ����ʽ��__________��
��2��Ϊ��ɴ�ʵ�飬����װ��A��B�⣬����ҪCװ�ã���װ����Ӧʢ__________����ҩƷ���ƣ�����װ���з�����Ӧ�Ļ�ѧ����ʽΪ__________��
��̽����������ͬѧ����ͼ��װ�ø�װ����ͼ��װ�ã�Aװ����ƿ�ڴ�������������CO��CO2��CH4�е�һ�ֻ��֣�Ϊȷ����ƿ������ijɷ֣�����ͬѧ��������ʵ�飺
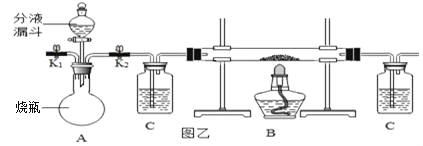
���ϣ�CH4��CuO�ڼ��������·�Ӧ������һ�ֽ������ʡ�������̼��ˮ��
��װ��B�IJ�������ʢ��������CuO���壻
��3.0g������NaOHŨ��Һͨ����Һ©��������ƿ�У���ַ�Ӧ��
��A��C��B��C������˳�����ӳ�װ��ͼ�ң���K1����K1��ͨ�뵪�����ٴ�K2������Bװ����������CuO���壬��ַ�Ӧ����Ӧǰװ���ڿ������ž�����
������Ӧ���������ƿ����Һ������Ϊ3.1g��Bװ���й��������������0.48g���ڶ���Cװ�õ�����������0.18g��
��3��д��CH4��CuO��Ӧ�Ļ�ѧ����ʽ__________��
��4������װ��C���Լ�Ӧ��ͬ����һ��װ��C���Լ���������__________��ͨ�����ݷ�������ƿ������ijɷ���__________��
��̽����������ͬѧ����ͼ��װ�ø�װ����ͼ��װ�ã�ʵ��ʱͨ��������CO���ԡ���������ͭ�ۡ�����������һϵ�е�̽����

��5���������ڷ�����Ӧ�Ļ�ѧ����ʽΪ__________����ʵ���һ������ȱ����__________��
��6��������ͬѧ���Բ�������ʣ��Ĺ��尴��ͼ�����̽���̽����
����ɫ��ҺB�е�������__________���ѧʽ����
��������ݸ���ͬѧ�ó���ʵ�����ݣ����������X��ͭ�����������Ƕ���__________����д��������̣�
����ʦ���ָ��ݸ���ͬѧ�����ݼ������ͭ���������������ƫ�������������ͬѧ�ڲ����д��ڵ�ʧ����__________��
���𰸡�2H2O2![]() 2H2O+O2��������ʯ��ˮ��Ca��OH��2+CO2�TCaCO3��+H2O��4CuO+CH4
2H2O+O2��������ʯ��ˮ��Ca��OH��2+CO2�TCaCO3��+H2O��4CuO+CH4![]() 4Cu+CO2+2H2O������ˮ������CO��CO2��CH4��Fe2O3+3CO
4Cu+CO2+2H2O������ˮ������CO��CO2��CH4��Fe2O3+3CO![]() 2Fe+3CO2��û�д���β����FeCl2��HCl��26.3%��û��ϴ�ӹ���C��
2Fe+3CO2��û�д���β����FeCl2��HCl��26.3%��û��ϴ�ӹ���C��
��������
��1��A�й��������ڶ������̴������·ֽ�����ˮ����������Ӧ�Ļ�ѧ����ʽ�ǣ�2H2O2![]() 2H2O+O2����
2H2O+O2����
��2��Ϊ��ɴ�ʵ�飬����װ��A��B�⣬����ҪCװ�ã���װ����Ӧʢ����ʯ��ˮ���������鷴Ӧ�Ƿ����ɶ�����̼����װ�����������ƺͶ�����̼��Ӧ����̼��Ƴ�����ˮ��������Ӧ�Ļ�ѧ����ʽΪ��Ca��OH��2+CO2�TCaCO3��+H2O��
��3��CH4��CuO��Ӧ�Ļ�ѧ����ʽΪ��4CuO+CH4![]() 4Cu+CO2+2H2O��
4Cu+CO2+2H2O��
��4������װ��C���Լ�Ӧ��ͬ��Ӧ����Ũ���ᣬ��һ��װ��C���Լ�������������ˮ������
ͨ�����ݷ�����֪�������ƿ����Һ������Ϊ3.1g��˵�������к��ж�����̼�����Ҷ�����̼������Ϊ��3.1g��3.0g=0.1g��
�ڶ���Cװ�õ�����������0.18g��˵�����������ͭ��Ӧ������0.18g��ˮ��
�跴Ӧ������ͭ����Ϊx��
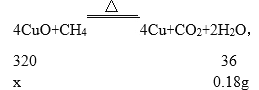
![]() =
=![]()
x=1.6g��
1.6g����ͭ����Ԫ������Ϊ��1.6g��![]() =0.32g��
=0.32g��
Bװ���й��������������0.48g��˵������ͭ����Ԫ������������0.48g����һ��˵������ͭ��һ����̼�����˷�Ӧ�����Һ�һ����̼��Ӧ����Ԫ������Ϊ��0.48g��0.32g=0.16g�������ƿ������ijɷ���CO��CO2��CH4��
��5������������������һ����̼��Ӧ�������Ͷ�����̼��������Ӧ�Ļ�ѧ����ʽΪ��Fe2O3+3CO![]() 2Fe+3CO2����ʵ���һ������ȱ����û�д���β����
2Fe+3CO2����ʵ���һ������ȱ����û�д���β����
��6������ɫ��Һ������ϡ���ᷴӦ���ɵ��Ȼ�������Һ��B�е�����������ϡ���ᷴӦ���ɵ��Ȼ������������Ȼ��⡣
����������Ϊy��
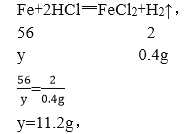
����C��ͭ��ͭ��������4g��
����X��ͭ�����������ǣ�![]() ��100%=26.3%��
��100%=26.3%��
�𣺹���X��ͭ������������26.3%��
����ʦ���ָ��ݸ���ͬѧ�����ݼ������ͭ���������������ƫ����ͬѧ�ڲ����д��ڵ�ʧ����û��ϴ�ӹ���C��