题目内容
【题目】某研究性小组对硫酸铵〔(NH4)2SO4〕化肥进行等级测定(该化肥中不存在其他含氮物质)。
【查阅资料】①氨气极易溶于水,其水溶液为氨水。氨水呈碱性,不稳定,易挥发。
②碱石灰是一种常见的干燥剂,其主要成分是CaO和NaOH固体混合物。
③硫酸铵化肥等级指标如下表:
指标项目 | 优等品 | 合格品 |
氮(N)含量 | ≥21.0% | ≥20.5% |
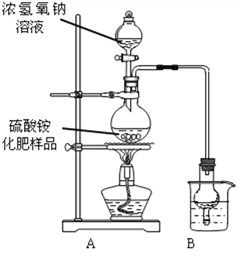
【实验设计】按右图所示装置进行实验。
(1)实验过程中,往烧瓶中加入足量浓氢氧化钠溶液,并加热使硫酸铵充分反应完全转化为NH3.
(2)B的作用是为了吸收产生的氨气。烧杯中最适宜的试剂是_________(填序号)
①水 ②浓HCl ③稀H2SO4 ④NaOH溶液
【交流讨论】实验小组同学认为用上述实验装置测得的硫酸铵化肥含氮量可能偏高,应在实验装置A、B之间增加一个装有______(填“浓硫酸”或“碱石灰”)的干燥装置。
【实验测定】经讨论后,他们改进了实验装置,排除了可能产生误差的因素,重新进行实验。取硫酸铵化肥样品13.5g进行实验,测得B装置增重3.4g。请通过计算判断该化肥的等级。________(写出计算过程)
【答案】 ③ 碱石灰 该化肥的等级是合格
【解析】【实验设计】(2)烧杯中的试剂是为了吸收氨气。由于硫酸能与氨气反应,所以最适宜用来吸收氨气的试剂是稀H2SO4;【交流讨论】实验小组的同学认为用上述实验装置测得的硫酸铵化肥含氮量可能偏高,由于硫酸能与氨气反应,需要在实验装置A、B之间增加一个装有碱石灰的干燥过程;【实验测定】设13.5g样品中含有(NH4)2SO4的质量为x,
(NH4)2SO4+2NaOH![]() Na2SO4+2H2O+2NH3↑
Na2SO4+2H2O+2NH3↑
132 34
x 3.4g
![]() ,解得:x=13.2g
,解得:x=13.2g
氮元素的质量是:![]() =2.8g
=2.8g
样品中氮元素的质量分数是: ![]() ≈20.7%,所以该化肥的等级是合格。
≈20.7%,所以该化肥的等级是合格。

 天天向上一本好卷系列答案
天天向上一本好卷系列答案 小学生10分钟应用题系列答案
小学生10分钟应用题系列答案【题目】碱石灰是CaO和NaOH固体的混合物,常用作干燥剂。碱石灰在空气中久置会吸收空气中的水和二氧化碳而变质。某实验小组为确定一瓶久置的碱石灰样品的成分,设计了如图所示实验流程。请你参与探究过程:

【查阅资料】①Ca(OH)2、Na2CO3溶于水无明显的温度变化;②CaCl2溶液呈中性。
(1)在操作一实验过程中,同学们发现向样品中加水时放出大量的热。据此实验,下列对样品成分分析正确的是________(填序号)。
A. 一定有NaOH B. 一定有Na2CO3 C. 一定有CaO D. 至少有NaOH、CaO中的一种
(2)在操作二之后所得的固体A中一定含有________。
(3)实验小组的同学继续对溶液B中的溶质进行了探究。
【猜想假设】猜想一:NaOH 猜想二:Na2CO3
猜想三:NaOH和Na2CO3 猜想四:Ca(OH)2和________
【实验验证】为进一步确认溶液B中溶质的成分,做了如下实验。
实验步骤 | 实验现象 | 实验结论 |
①取少量溶液B于试管中,加入足量CaCl2溶液; ②过滤,用pH试纸检测滤液的pH | ①__________________; ②pH>7 | 猜想三正确 |
实验步骤①中发生的化学反应方程式是________________________________,其实验目的是________________________________。
【反思评价】对于像碱石灰这样容易变质的物质,保存时需要注意密封保存。